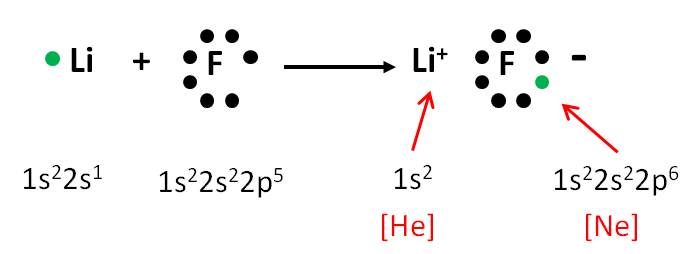
Yoduro De Litio Estructura De Lewis

El yoduro de litio (LiI) es un compuesto iónico. Para entender su comportamiento, es fundamental dibujar su Estructura de Lewis. ¡Vamos a hacerlo paso a paso!
¿Qué es una Estructura de Lewis?
Una Estructura de Lewis es un diagrama que muestra cómo se enlazan los átomos en una molécula, y cómo se distribuyen los electrones de valencia (los electrones del último nivel de energía) alrededor de cada átomo. Es una forma visual de representar los enlaces químicos.
Pasos para Dibujar la Estructura de Lewis de LiI
Paso 1: Identificar los Átomos y sus Electrones de Valencia.
- Litio (Li): Pertenece al grupo 1, por lo que tiene 1 electrón de valencia.
- Yodo (I): Pertenece al grupo 17 (o 7A), por lo que tiene 7 electrones de valencia.
Paso 2: Determinar la Carga de los Iones.
Como LiI es un compuesto iónico, el litio (Li) cede su electrón al yodo (I) para alcanzar una configuración electrónica estable (como la de un gas noble).
- Li pierde 1 electrón, formando el catión Li+.
- I gana 1 electrón, formando el anión I-.
Paso 3: Dibujar los Iones.
- Li+: Al perder su electrón de valencia, ya no tiene electrones que dibujar alrededor. Simplemente escribimos Li+.
- I-: Al ganar un electrón, ahora tiene 8 electrones de valencia. Dibujamos el símbolo del yodo (I) rodeado de 8 puntos (o cruces) que representan los electrones, y encerramos todo entre corchetes con una carga negativa: [ :I: ]- .
¡Importante! Cada punto representa un electrón. Los electrones se agrupan de a pares siempre que sea posible.
Paso 4: La Estructura Completa.
La estructura de Lewis completa para el yoduro de litio se representa como: Li+ [ :I: ]-.
¿Por qué es importante esto?
La Estructura de Lewis de LiI nos ayuda a entender que:
- El enlace entre el litio y el yodo es un enlace iónico, formado por la transferencia de electrones.
- El yodo, al ganar un electrón, adquiere una configuración electrónica estable, similar a la de un gas noble.
- El litio, al perder su electrón, también alcanza una configuración electrónica estable.
Ejemplo Práctico
Imagina que el litio es una persona que tiene una canica (su electrón de valencia). El yodo es otra persona que necesita una canica más para completar un juego. El litio le da su canica al yodo. Ahora el litio ya no tiene canicas (Li+), y el yodo tiene todas las que necesita (I-). ¡Ambos están contentos!
En resumen
La Estructura de Lewis de LiI es una representación visual simple pero poderosa de la transferencia de electrones que ocurre en la formación del enlace iónico. Comprender este concepto es crucial para comprender la química de muchos otros compuestos.