Tabla Periodica Representativos Y De Transicion

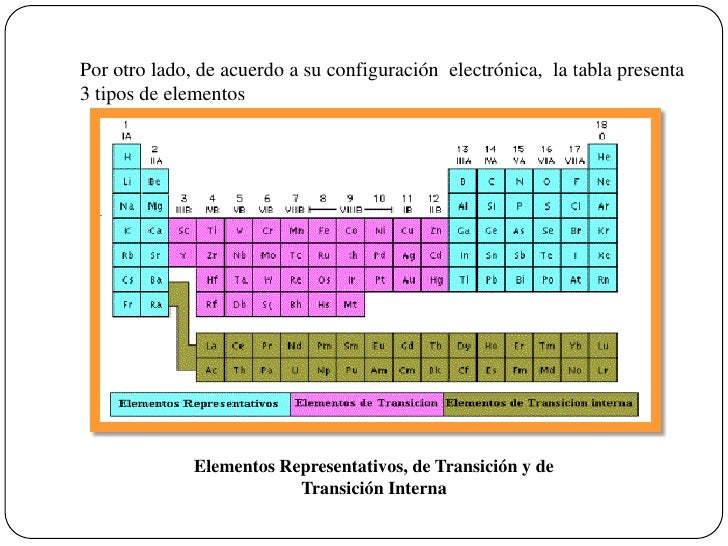
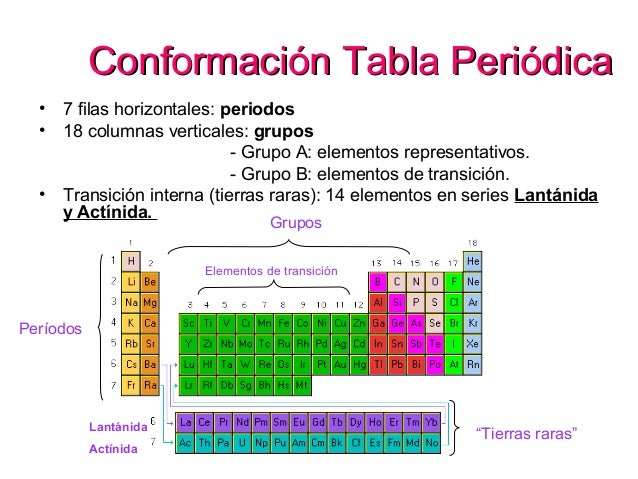
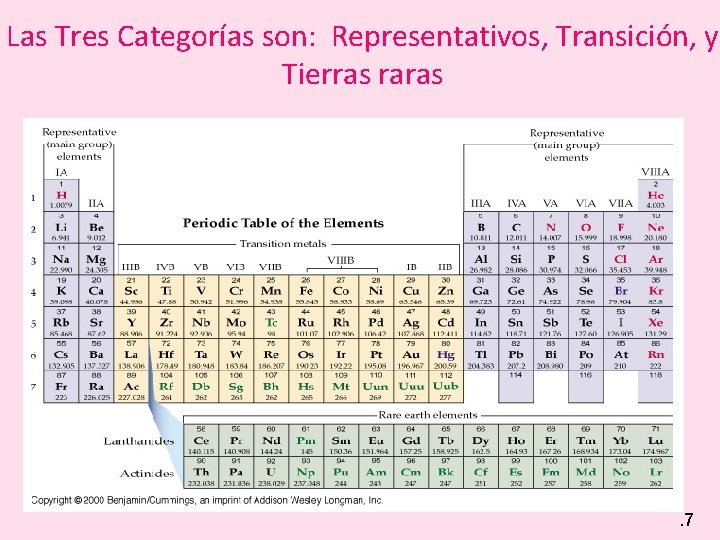
La tabla periódica organiza los elementos químicos según sus propiedades. Se divide en bloques, y dentro de estos bloques, podemos identificar los elementos representativos y los elementos de transición.
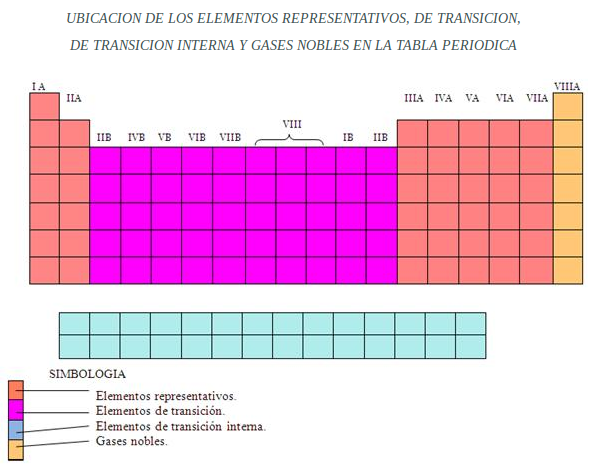
Los elementos representativos, también conocidos como elementos de los grupos principales, se encuentran en los grupos 1, 2 y del 13 al 18 (1A, 2A, 3A al 8A). Sus propiedades químicas son bastante predecibles y fáciles de entender. Sus electrones de valencia (los electrones en la capa más externa) se encuentran en los orbitales s y p.
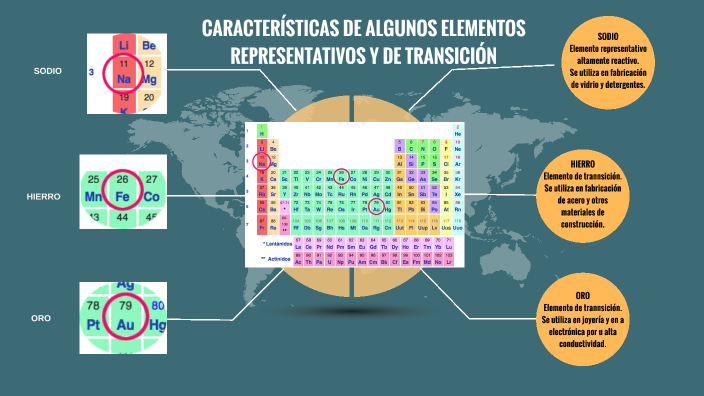
Ejemplos de elementos representativos: Sodio (Na), Magnesio (Mg), Aluminio (Al), Carbono (C), Oxígeno (O) y Cloro (Cl).
Estos elementos tienden a formar iones con cargas predecibles. Por ejemplo, el Sodio (Na) comúnmente pierde un electrón para formar el ion Na+, mientras que el Cloro (Cl) gana un electrón para formar el ion Cl-.
En contraste, los elementos de transición se encuentran en los grupos 3 al 12 (grupos B en algunas notaciones más antiguas). Sus propiedades son menos predecibles que las de los elementos representativos, y muestran una variedad de estados de oxidación (cargas). Sus electrones de valencia se encuentran en los orbitales d y s.
Ejemplos de elementos de transición: Hierro (Fe), Cobre (Cu), Oro (Au), Plata (Ag), Níquel (Ni) y Zinc (Zn).
Una característica importante de los elementos de transición es su capacidad para formar iones coloreados en solución. El color se debe a transiciones electrónicas entre los orbitales d.
Los elementos de transición interna, también llamados lantánidos y actínidos, se encuentran debajo del cuerpo principal de la tabla periódica. Son similares a los elementos de transición en que también muestran múltiples estados de oxidación y a menudo forman iones coloreados.
En resumen, los elementos representativos tienen propiedades más predecibles y sus electrones de valencia se encuentran en los orbitales s y p, mientras que los elementos de transición muestran una mayor variedad de propiedades y sus electrones de valencia se encuentran en los orbitales d y s.