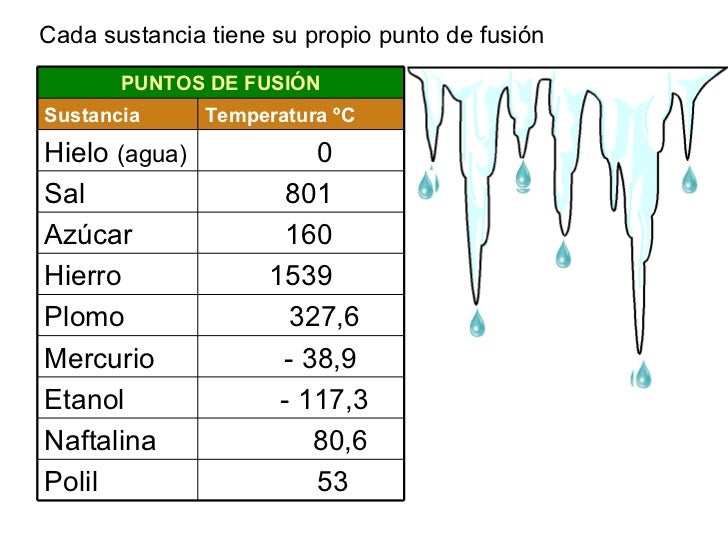
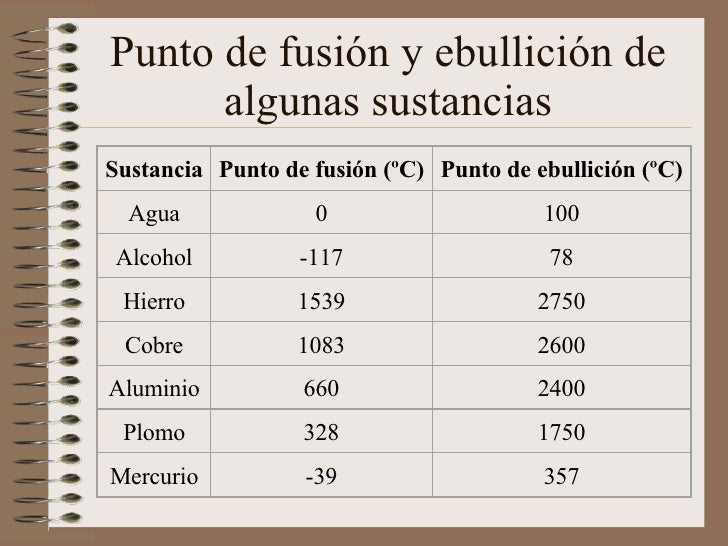
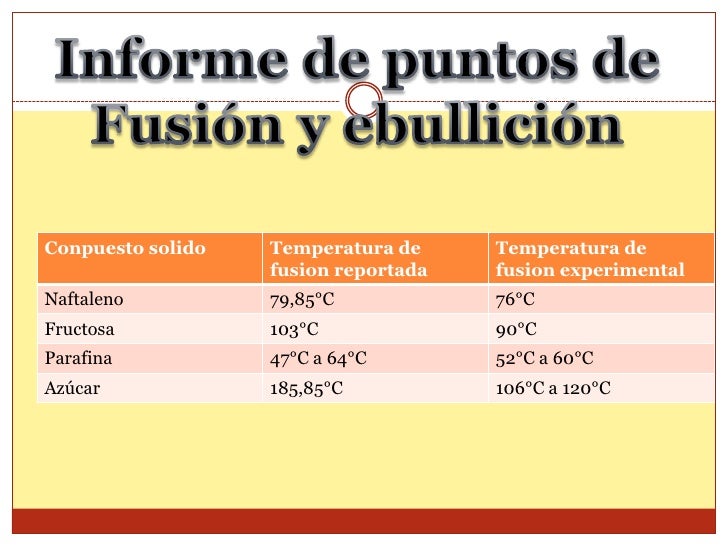
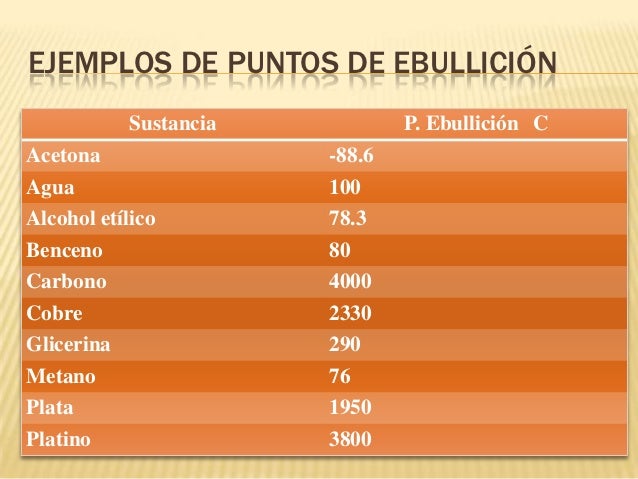
Tabla De Punto De Fusión Y Ebullición
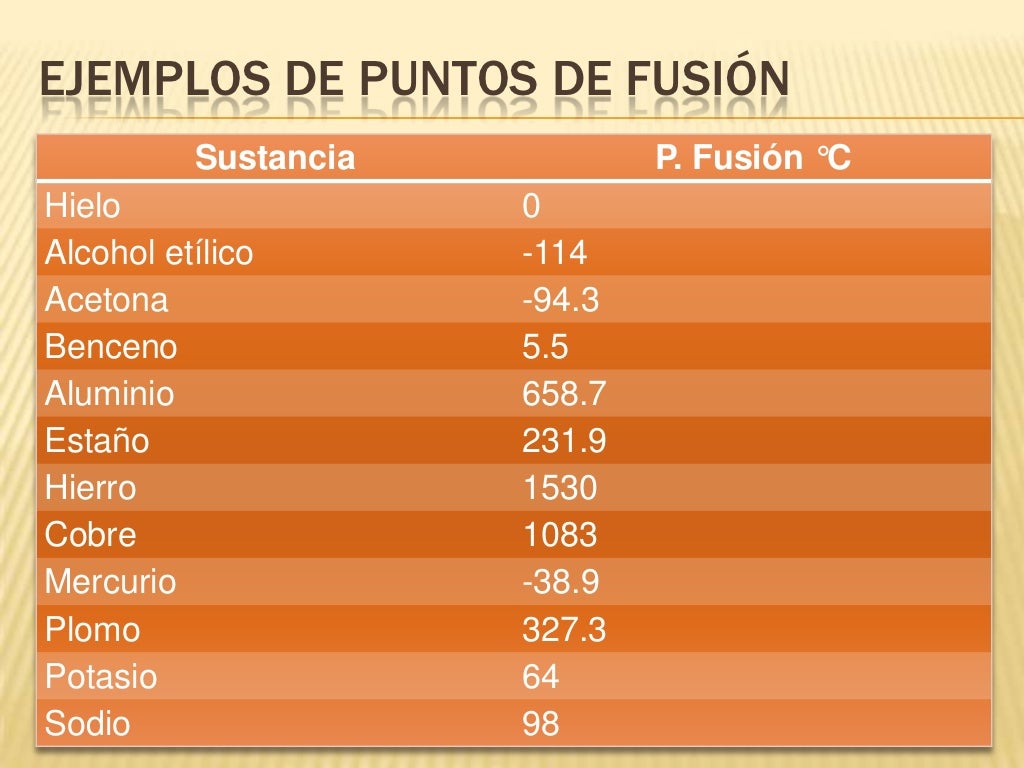
Analizar y resolver una tabla de puntos de fusión y ebullición implica un proceso cuidadoso. Empecemos con la recolección de datos. Reunir todos los puntos de fusión y ebullición relevantes es el primer paso.
Identificar las sustancias presentes en la tabla es crucial. Observar las unidades de medida (e.g., °C, K) también es importante. Asegúrate de que todas las unidades sean consistentes para evitar errores.
Organización y Análisis Inicial
Organizar los datos en un formato claro facilita la comparación. Se puede usar una tabla con columnas para sustancia, punto de fusión, y punto de ebullición. Un formato digital (hoja de cálculo) es altamente recomendable.
Analizar las tendencias en los datos es esencial. ¿Existen patrones entre las sustancias y sus puntos de fusión/ebullición? Considera el tipo de enlace químico (iónico, covalente, metálico) presente.
Investigar la estructura molecular de cada sustancia ayuda mucho. Esto puede dar pistas sobre las fuerzas intermoleculares. Las fuerzas intermoleculares influyen directamente en los puntos de fusión y ebullición.
Identificación de Suposiciones
Es importante identificar las suposiciones que estamos haciendo. Asumimos que las sustancias son puras y no mezclas. La presencia de impurezas alteraría los puntos de fusión y ebullición.
Asumimos que la presión es constante (normalmente 1 atm). Los puntos de fusión y ebullición varían con la presión. Una presión diferente implicaría valores diferentes.
También asumimos un conocimiento básico de química. Entendemos los tipos de enlaces y las fuerzas intermoleculares. Sin este conocimiento, el análisis sería incompleto.
Evaluación de Opciones y Solución
Ante una pregunta específica, evalúa las opciones disponibles. Por ejemplo, "¿Qué sustancia tiene el punto de ebullición más alto?". Compara los valores de la tabla para responder.
Si se te pide predecir el estado físico a una temperatura dada, compara esa temperatura con los puntos de fusión y ebullición. Si la temperatura está por debajo del punto de fusión, es sólido. Si está entre el punto de fusión y ebullición, es líquido. Si está por encima del punto de ebullición, es gaseoso.
Para resolver problemas más complejos, aplica principios de química. Considera la polaridad de las moléculas y su efecto en las fuerzas intermoleculares. Una molécula más polar tendrá mayores fuerzas intermoleculares.
Conclusión Razonada
Después del análisis y la evaluación, llega a una conclusión razonada. Justifica tu respuesta con evidencia de la tabla y principios químicos. Evita conclusiones precipitadas sin fundamento.
Verifica tu respuesta y asegúrate de que tenga sentido químico. ¿La respuesta concuerda con las tendencias observadas y el tipo de sustancia? Una revisión final es fundamental para minimizar errores.
Finalmente, comunica tus resultados de manera clara y concisa. Explica el proceso que seguiste y las razones para tu conclusión. Una comunicación efectiva es clave para demostrar tu comprensión.