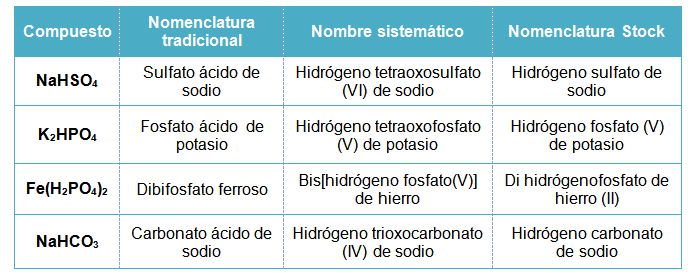
Sales Acidas Ejemplos Con Las 3 Nomenclaturas
+Nomenclatura+tradicional:+Nomenclatura+Stock:.jpg)
Las sales ácidas son compuestos químicos fascinantes. Son el resultado de la neutralización incompleta de un ácido poliprótico por una base. Piensa en ellas como una parada a medio camino en la reacción entre un ácido y una base. Aprendamos a identificarlas y nombrarlas usando las tres nomenclaturas principales.
¿Qué son las Sales Ácidas?
Una sal ácida contiene un átomo de hidrógeno (H+) que puede ser reemplazado por un metal para formar una sal neutra. En otras palabras, aún conserva la capacidad de reaccionar como un ácido.
Nomenclaturas: Un Mapa para Nombrar
Existen tres sistemas principales para nombrar sales ácidas: Nomenclatura tradicional (o clásica), Nomenclatura Stock y Nomenclatura Sistemática (o IUPAC). Cada una tiene sus reglas y te las explicaremos paso a paso.
1. Nomenclatura Tradicional (Clásica)
Esta nomenclatura usa prefijos como bi- o di- (para dos hidrógenos), tri- (para tres hidrógenos), etc., para indicar la cantidad de hidrógenos presentes. Además, se emplean las terminaciones -oso o -ico dependiendo de la valencia del metal.
Ejemplo: HSO4-
Nombre: Bisulfato (o Sulfato ácido)
En este caso, "bi-" indica que hay un hidrógeno presente en el anión sulfato.
2. Nomenclatura Stock
La nomenclatura Stock es más sencilla. Indica el estado de oxidación del metal (si lo hay) con números romanos entre paréntesis después del nombre del metal.
Ejemplo: KHCO3
Nombre: Hidrogenocarbonato de potasio
También puede nombrarse: Carbonato ácido de potasio
Aquí, simplemente se indica que es un hidrogenocarbonato (o carbonato ácido) y se especifica el metal, el potasio, sin necesidad de indicar su estado de oxidación ya que solo tiene uno.
3. Nomenclatura Sistemática (IUPAC)
La nomenclatura IUPAC es la más precisa y utiliza prefijos numéricos (mono-, di-, tri-, tetra-, etc.) para indicar la cantidad de hidrógenos y otros elementos presentes.
Ejemplo: NaH2PO4
Nombre: Dihidrogenofosfato de sodio
Aquí, "dihidrogeno-" indica la presencia de dos hidrógenos en el fosfato. Luego se especifica el anión fosfato y finalmente el catión sodio.
Más Ejemplos Prácticos
- NaHCO3: Bicarbonato de sodio (Tradicional), Hidrogenocarbonato de sodio (Stock), Monohidrogenocarbonato de sodio (IUPAC).
- NaHS: Bisulfuro de sodio (Tradicional), Hidrogenosulfuro de sodio (Stock), Monohidrogenosulfuro de sodio (IUPAC).
- Ca(HSO3)2: Bisulfito de calcio (Tradicional), Hidrogenosulfito de calcio (Stock), Bis[trioxidohidrosulfato(1-)] de calcio (IUPAC - puede ser más complejo en algunos casos).
Conclusión
Comprender las sales ácidas y las diferentes nomenclaturas es fundamental en química. Con práctica y ejemplos, podrás identificar y nombrar estos compuestos con facilidad. ¡No te desanimes! Recuerda que cada nomenclatura tiene su lógica y, una vez que la entiendas, será mucho más sencillo.
+Nomenclatura+sistemática:.jpg)