Que Tipo De Enlace Es El Amoniaco
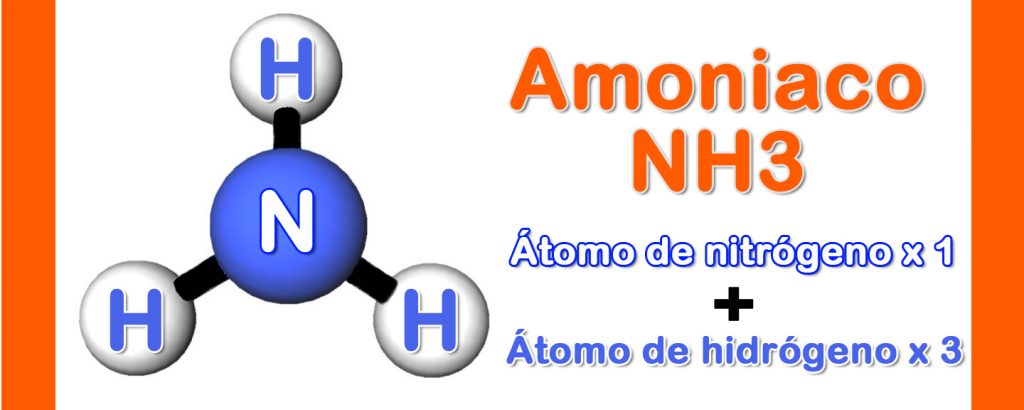
El amoniaco, con su fórmula química NH3, es un compuesto crucial en diversas áreas, desde la agricultura hasta la limpieza. Comprender el tipo de enlace que mantiene unidos sus átomos es fundamental para entender sus propiedades y comportamiento.
¿Qué es un Enlace Químico?
Un enlace químico es la fuerza que mantiene unidos a los átomos para formar moléculas o compuestos. Esta fuerza surge de la interacción entre los electrones de los átomos. Hay varios tipos de enlaces químicos, cada uno con características distintas. El tipo de enlace determina muchas propiedades de la sustancia, como su punto de fusión, punto de ebullición y solubilidad.
El Enlace Covalente en el Amoniaco
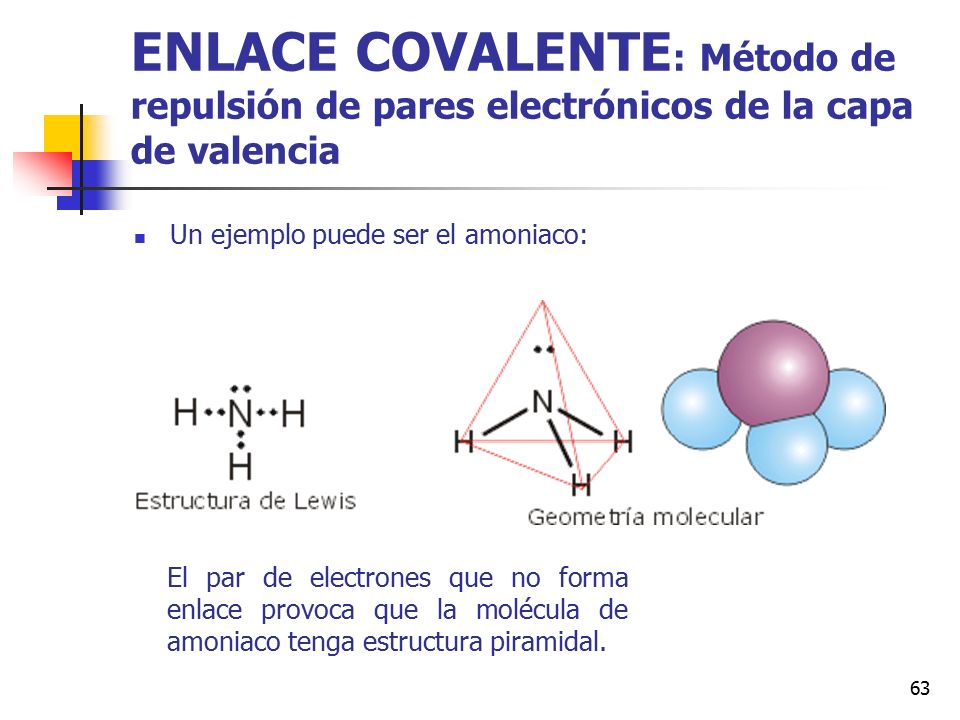
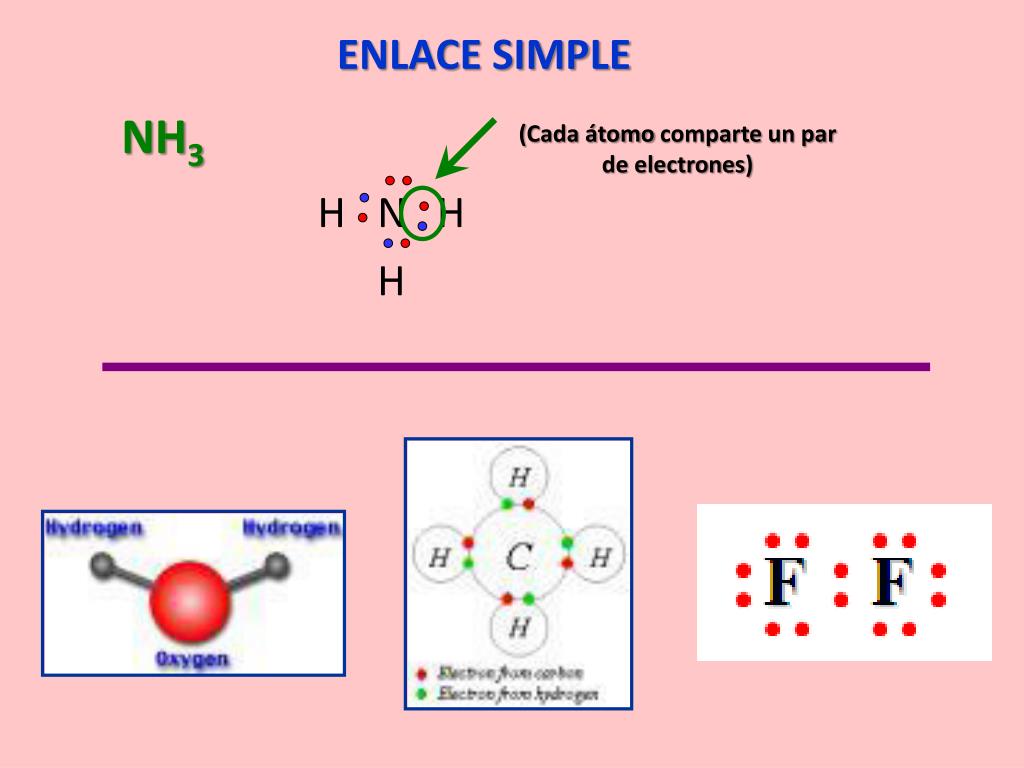
El amoniaco está formado por un átomo de nitrógeno (N) y tres átomos de hidrógeno (H). El enlace predominante en la molécula de amoniaco es el enlace covalente.
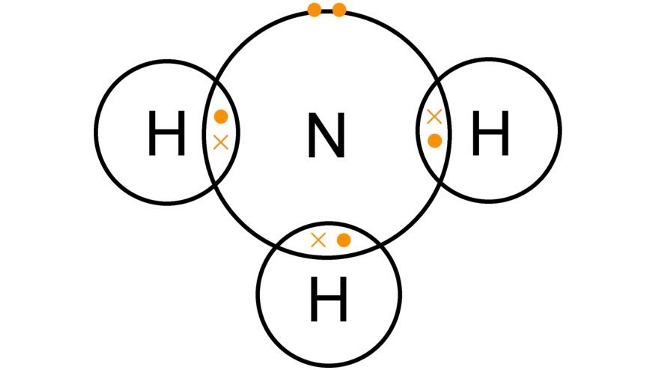
Un enlace covalente se forma cuando dos átomos comparten electrones para alcanzar una configuración electrónica más estable. En lugar de transferir electrones (como en un enlace iónico), los átomos comparten los electrones para completar sus capas de valencia.
El nitrógeno tiene 5 electrones en su capa de valencia y necesita 3 electrones más para completar el octeto (8 electrones). Cada átomo de hidrógeno tiene 1 electrón y necesita 1 más para alcanzar una configuración estable de 2 electrones (como el helio).
Enlace Covalente Polar
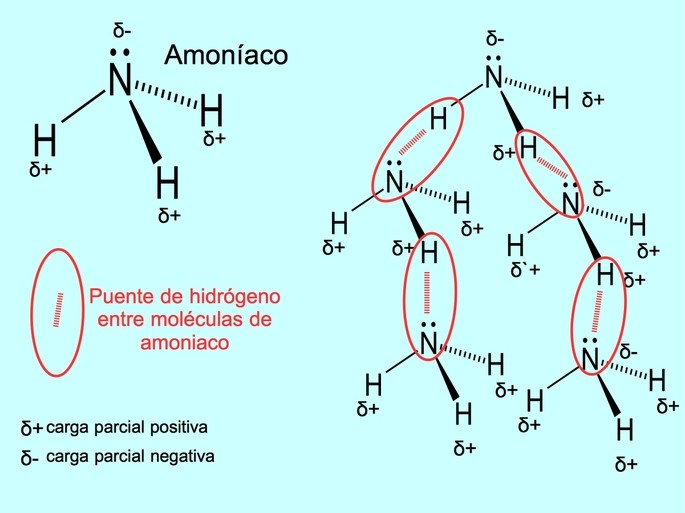
En el amoniaco, el enlace covalente es específicamente un enlace covalente polar. Esto significa que los electrones no se comparten de manera equitativa entre el nitrógeno y el hidrógeno.
El nitrógeno es más electronegativo que el hidrógeno. La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí en un enlace químico. Debido a su mayor electronegatividad, el nitrógeno atrae los electrones compartidos con mayor fuerza.
Como resultado, el nitrógeno adquiere una carga parcial negativa (δ-) y cada hidrógeno adquiere una carga parcial positiva (δ+). Esta distribución desigual de la carga crea un dipolo en cada enlace N-H.
La Geometría Molecular y la Polaridad del Amoniaco
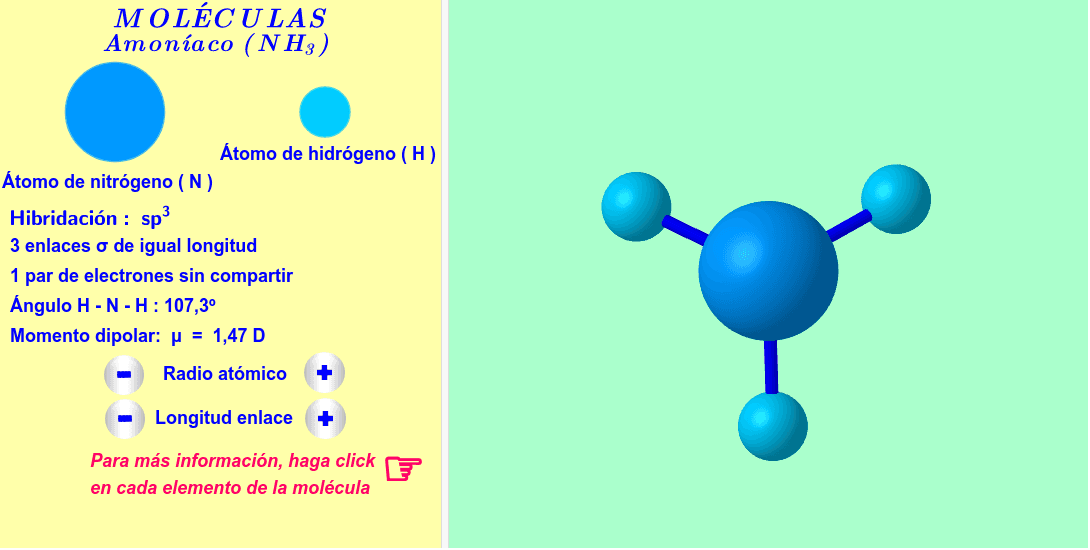
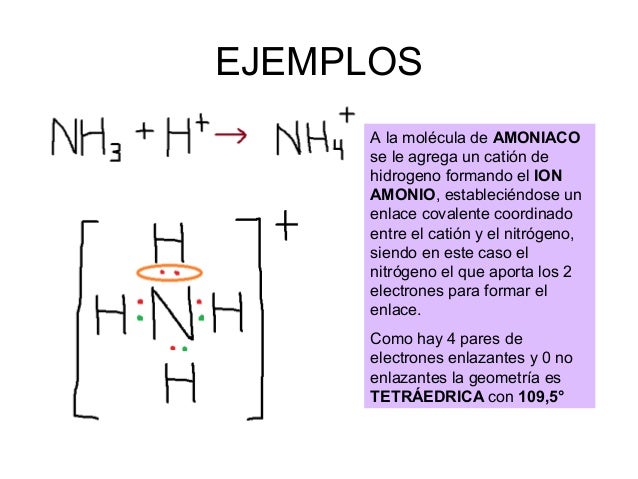
La forma de la molécula de amoniaco también contribuye a su polaridad. El amoniaco tiene una geometría piramidal trigonal.
Esto significa que los tres átomos de hidrógeno se encuentran en la base de una pirámide y el átomo de nitrógeno está en la cima. La presencia de un par de electrones no enlazantes en el nitrógeno también influye en esta geometría.
Debido a esta forma y la polaridad de los enlaces N-H, los dipolos individuales de los enlaces no se cancelan. Esto resulta en una molécula de amoniaco polar en general, con un extremo parcialmente negativo (el nitrógeno) y un extremo parcialmente positivo (los hidrógenos).
Aplicaciones y Relevancia del Amoniaco
La polaridad del amoniaco es crucial para muchas de sus propiedades y aplicaciones. Por ejemplo, el amoniaco es muy soluble en agua debido a su capacidad para formar enlaces de hidrógeno con las moléculas de agua.
El amoniaco se utiliza principalmente como fertilizante en la agricultura. También se utiliza en la producción de plásticos, fibras sintéticas y explosivos. En la limpieza doméstica, el amoniaco se utiliza en algunos productos para eliminar manchas y grasas.
En resumen, el amoniaco es un compuesto vital con enlaces covalentes polares. La polaridad y la geometría molecular de la molécula son clave para comprender sus propiedades y su amplia gama de aplicaciones.