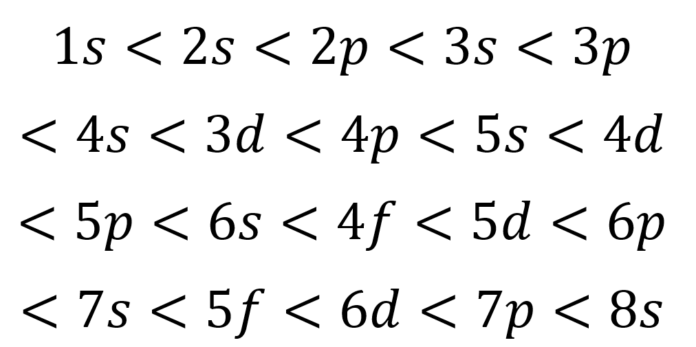Que Nos Dice El Principio De Aufbau
¡Hola! Hoy vamos a explorar un principio fundamental de la química: el Principio de Aufbau. No te preocupes, suena complicado, pero lo vamos a simplificar. Verás que es más fácil de lo que parece.
¿Qué es el Principio de Aufbau?
El Principio de Aufbau, también conocido como el principio de la construcción, nos dice cómo se llenan los orbitales atómicos con electrones. Imagina que estás construyendo una casa. No empiezas con el techo, ¿verdad? Primero pones los cimientos, luego las paredes, y así sucesivamente.
De manera similar, los electrones llenan los orbitales atómicos en un orden específico. El Principio de Aufbau nos ayuda a predecir ese orden. Este orden minimiza la energía del átomo. Es como buscar la forma más estable de construir tu casa.
Definiciones Clave
Antes de continuar, aclaremos algunos términos importantes:
- Átomo: La unidad básica de la materia. Todo a tu alrededor está hecho de átomos.
- Electrón: Una partícula con carga negativa que gira alrededor del núcleo del átomo. Piensa en ellos como los "ladrillos" que llenan los orbitales.
- Orbital Atómico: Una región alrededor del núcleo donde es más probable encontrar un electrón. No son órbitas circulares como los planetas alrededor del sol. Son regiones tridimensionales con diferentes formas.
- Nivel de Energía: Los orbitales se organizan en niveles de energía. Cuanto más cerca del núcleo, menor es la energía. Imagina pisos en un edificio; los de abajo son más fáciles de alcanzar.
La Regla de Madelung (o la Regla n + l)
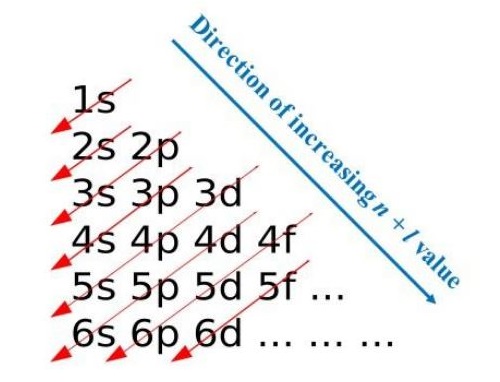
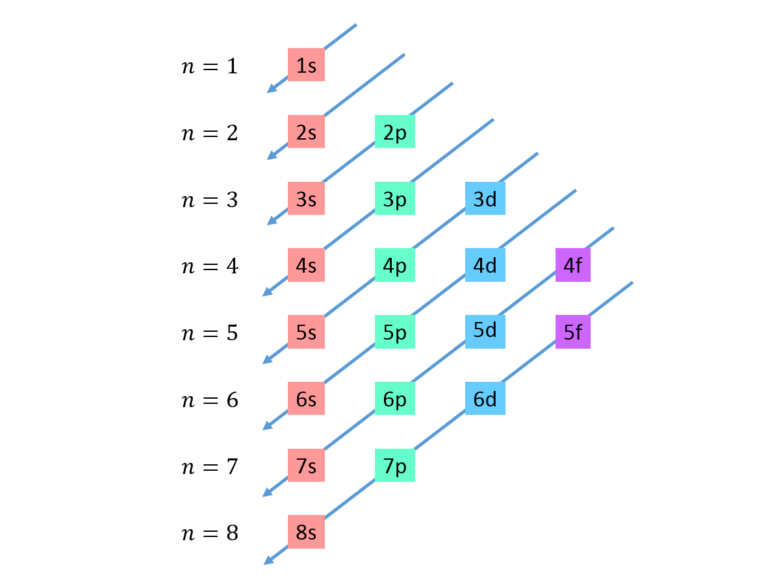
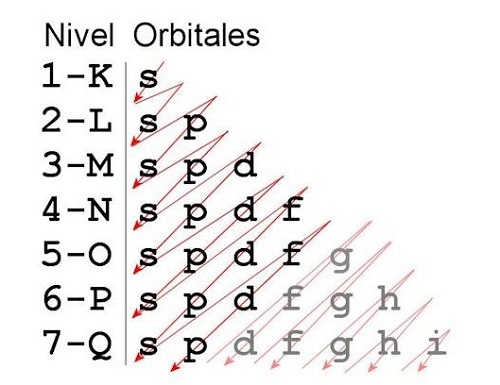
Para saber qué orbital se llena primero, utilizamos la Regla de Madelung, también conocida como la regla (n + l). Esta regla dice que los orbitales se llenan en orden creciente de la suma de sus números cuánticos principal (n) y azimutal (l).
¿Qué significan n y l? No te asustes. 'n' representa el nivel de energía principal (1, 2, 3, etc.). 'l' representa la forma del orbital (0 para s, 1 para p, 2 para d, 3 para f). El orbital con el menor valor de (n + l) se llena primero.
Si dos orbitales tienen el mismo valor de (n + l), entonces se llena primero el orbital con el menor valor de 'n'. Es como si, al construir tu casa, primero llenaras los pisos inferiores antes de pasar a los superiores.
Ejemplos Prácticos
Veamos algunos ejemplos para que quede más claro. Comparemos el orbital 3d y el 4s.
- Para el orbital 3d: n = 3, l = 2. Entonces, n + l = 3 + 2 = 5
- Para el orbital 4s: n = 4, l = 0. Entonces, n + l = 4 + 0 = 4
El orbital 4s tiene un valor de (n + l) menor (4) que el orbital 3d (5). Por lo tanto, el orbital 4s se llena antes que el orbital 3d. Aunque el 3d tiene un nivel de energía "menor" (3), la suma de n+l es lo que determina el orden.
Otro ejemplo: Comparemos 2p y 3s.
- Para el orbital 2p: n = 2, l = 1. Entonces, n + l = 2 + 1 = 3
- Para el orbital 3s: n = 3, l = 0. Entonces, n + l = 3 + 0 = 3
Ambos tienen el mismo valor de (n + l). En este caso, se llena primero el orbital con el menor valor de 'n', que es 2p. Así que, 2p se llena antes que 3s.
En Resumen
El Principio de Aufbau nos ayuda a entender cómo los electrones se distribuyen en los orbitales atómicos. Usamos la Regla de Madelung (n + l) para predecir el orden de llenado. Recuerda, la clave es buscar la configuración electrónica más estable y de menor energía. Al comprender este principio, podrás predecir las propiedades químicas de los elementos.
¡Espero que esto te haya ayudado a comprender mejor el Principio de Aufbau! ¡Sigue explorando la química!