Punto De Ebullicion Del Dietil Eter

¡Hola, futuros químicos! Vamos a repasar el punto de ebullición del dietil éter. No te preocupes, ¡lo haremos juntos y de forma sencilla! Preparémonos para el examen.
¿Qué es el Dietil Éter?
Primero, ¿qué es exactamente el dietil éter? Es un compuesto orgánico. Su fórmula química es (C2H5)2O. También se le conoce como éter etílico. Es un líquido incoloro con un olor característico.
El dietil éter es muy volátil. Esto significa que se evapora fácilmente a temperatura ambiente. Además, es inflamable, ¡así que hay que tener cuidado al manejarlo! Se usa comúnmente como disolvente en laboratorios y en la industria.
Punto de Ebullición: Definición Clave
El punto de ebullición es la temperatura. A esta temperatura, un líquido cambia a estado gaseoso. Es específico para cada sustancia. Depende de las fuerzas intermoleculares.
Las fuerzas intermoleculares son las atracciones entre las moléculas. Cuanto más fuertes sean estas fuerzas, mayor será el punto de ebullición. Recuerda esto: ¡más fuerza, más calor!
El Punto de Ebullición del Dietil Éter
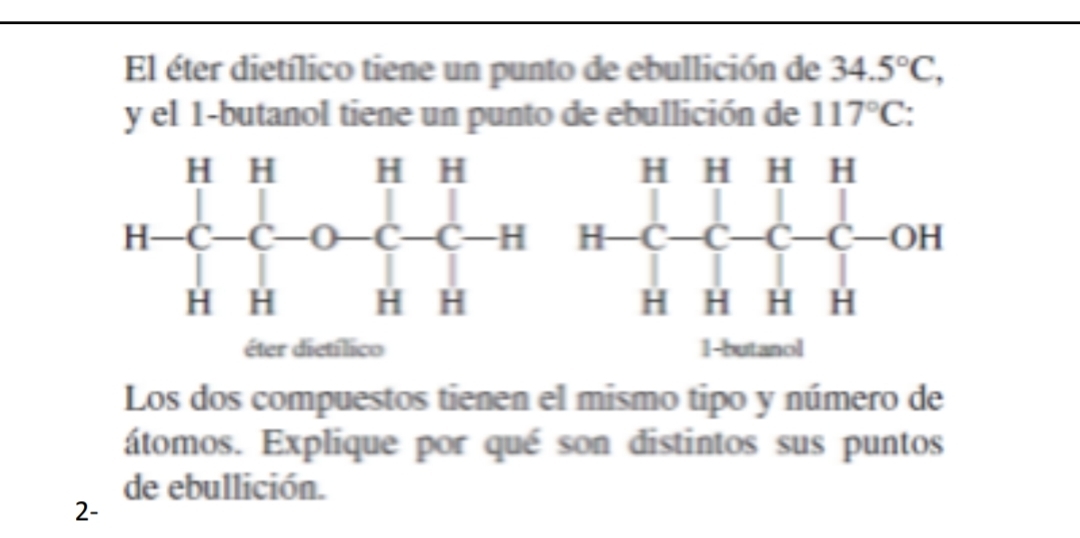
El punto de ebullición del dietil éter es de 34.6 °C (aproximadamente 94.3 °F). Es un valor importante. Se debe recordar para el examen. Es relativamente bajo comparado con otros compuestos similares.
¿Por qué es tan bajo? La respuesta está en sus fuerzas intermoleculares. El dietil éter tiene principalmente fuerzas de Van der Waals. Estas fuerzas son débiles. No forma enlaces de hidrógeno significativos consigo mismo.
Fuerzas Intermoleculares y Punto de Ebullición
Comparemos el dietil éter con el etanol. El etanol (alcohol etílico) tiene un punto de ebullición mucho más alto. ¿Por qué? El etanol puede formar enlaces de hidrógeno.
Los enlaces de hidrógeno son más fuertes que las fuerzas de Van der Waals. Por lo tanto, se necesita más energía (calor) para romperlos. Esto eleva el punto de ebullición del etanol. El dietil éter solo posee las débiles fuerzas de Van der Waals.
Factores que Afectan el Punto de Ebullición
Además de las fuerzas intermoleculares, otros factores pueden influir. La presión atmosférica es uno de ellos. A menor presión, menor será el punto de ebullición.
A nivel del mar, la presión es mayor. En la cima de una montaña, la presión es menor. Por lo tanto, el dietil éter hervirá a una temperatura ligeramente inferior en la cima de una montaña.
Resumen y Consejos para el Examen
Repasemos los puntos clave. El dietil éter es (C2H5)2O. Su punto de ebullición es de 34.6 °C. Se debe a sus débiles fuerzas de Van der Waals.
Recuerda comparar el dietil éter con el etanol. El etanol tiene enlaces de hidrógeno más fuertes. La presión también influye. Menor presión, menor punto de ebullición.
¡Estudia con confianza! Repasa tus apuntes. Haz ejercicios de práctica. ¡Vas a tener éxito en el examen! ¡Ánimo!