Propiedades Quimicas Y Su Variacion Periodica
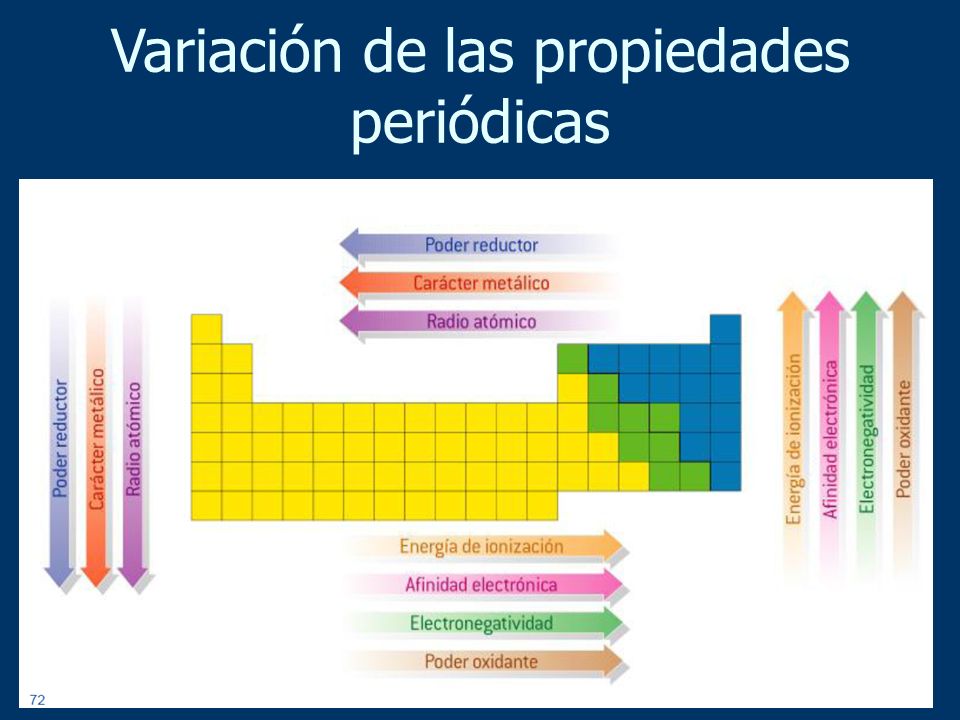
Las propiedades químicas describen cómo una sustancia reacciona con otras sustancias. Indican si una sustancia es inflamable, corrosiva o reactiva. Piensa en ello como la "personalidad" química de un elemento.
¿Qué significa "variación periódica"?
La variación periódica se refiere a las tendencias que muestran las propiedades químicas y físicas de los elementos en la tabla periódica. Estas tendencias se repiten a medida que avanzamos a lo largo de la tabla. Observar estas tendencias nos ayuda a predecir cómo se comportarán los elementos.
Electronegatividad: La "atracción" de los electrones
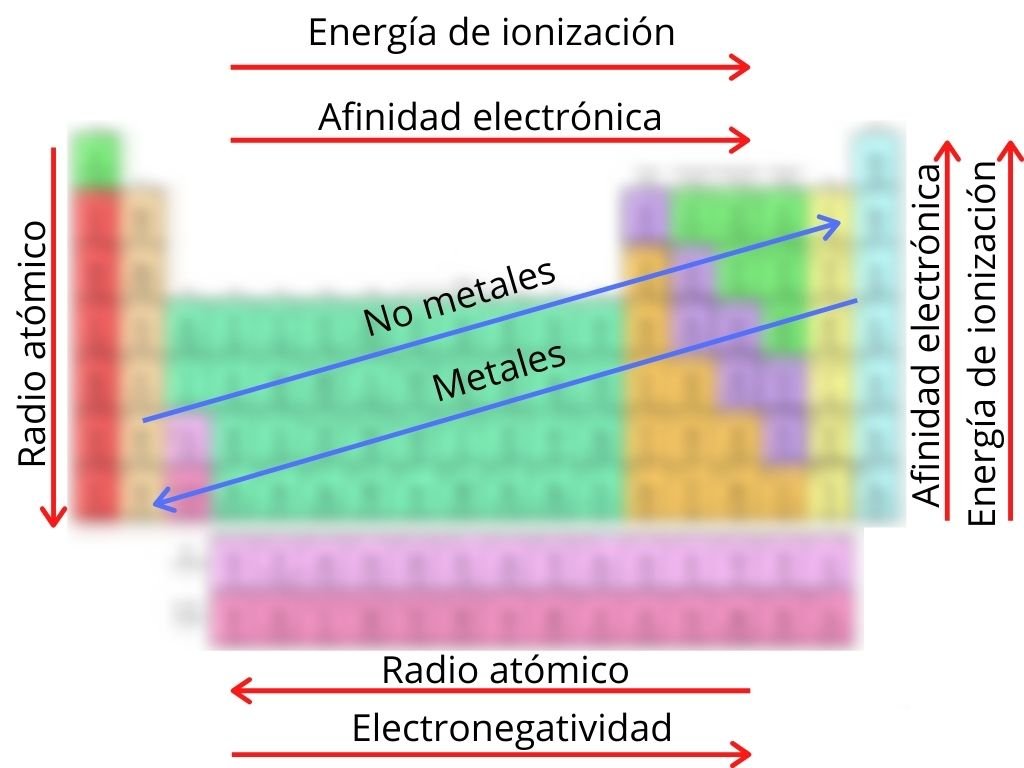
La electronegatividad mide la capacidad de un átomo para atraer electrones hacia sí mismo en un enlace químico. Un elemento con alta electronegatividad "quiere" electrones con más fuerza. Por ejemplo, el flúor es el elemento más electronegativo.
Tendencia periódica: La electronegatividad generalmente aumenta de izquierda a derecha en un período y disminuye de arriba hacia abajo en un grupo (o familia).
Ejemplo: El oxígeno es más electronegativo que el carbono. Esto significa que, en un enlace entre oxígeno y carbono, el oxígeno atraerá los electrones compartidos con más fuerza.
Radio Atómico: El tamaño importa
El radio atómico es una medida del tamaño de un átomo. Es la mitad de la distancia entre los núcleos de dos átomos idénticos unidos químicamente.
Tendencia periódica: El radio atómico generalmente disminuye de izquierda a derecha en un período (debido al aumento de la carga nuclear efectiva) y aumenta de arriba hacia abajo en un grupo (debido a la adición de nuevas capas de electrones).
Ejemplo: El sodio (Na) es más grande que el cloro (Cl). El potasio (K) es más grande que el sodio (Na).
Energía de Ionización: ¿Cuánto cuesta quitar un electrón?
La energía de ionización es la energía necesaria para remover un electrón de un átomo neutro en estado gaseoso. Cuanto mayor sea la energía de ionización, más difícil será remover el electrón.
Tendencia periódica: La energía de ionización generalmente aumenta de izquierda a derecha en un período y disminuye de arriba hacia abajo en un grupo.
Ejemplo: Es más fácil remover un electrón del sodio (Na) que del cloro (Cl). El helio (He) tiene una energía de ionización muy alta, lo que lo hace muy estable e inerte.
Afinidad Electrónica: ¿Cuánto "le gusta" ganar un electrón?
La afinidad electrónica es el cambio de energía cuando un átomo neutro en estado gaseoso gana un electrón. Un valor negativo indica que el átomo "quiere" ganar un electrón (se libera energía).
Tendencia periódica: Generalmente, la afinidad electrónica se vuelve más negativa (libera más energía) de izquierda a derecha en un período, aunque hay muchas excepciones. La tendencia en un grupo no es tan clara.
Ejemplo: El cloro (Cl) tiene una alta afinidad electrónica; le gusta ganar electrones para formar un ion cloruro (Cl-).
Reactividad: La "disposición" a reaccionar
La reactividad describe la facilidad con la que un elemento reacciona químicamente con otras sustancias. La reactividad está estrechamente relacionada con las otras propiedades periódicas mencionadas.
Ejemplo: Los metales alcalinos (Grupo 1) son muy reactivos porque tienen una baja energía de ionización y pierden fácilmente un electrón. Los gases nobles (Grupo 18) son muy poco reactivos porque tienen capas de electrones completas.
Entender estas tendencias periódicas es fundamental para predecir y comprender el comportamiento químico de los elementos.