Problemas Que Involucran Cambios De Temperatura
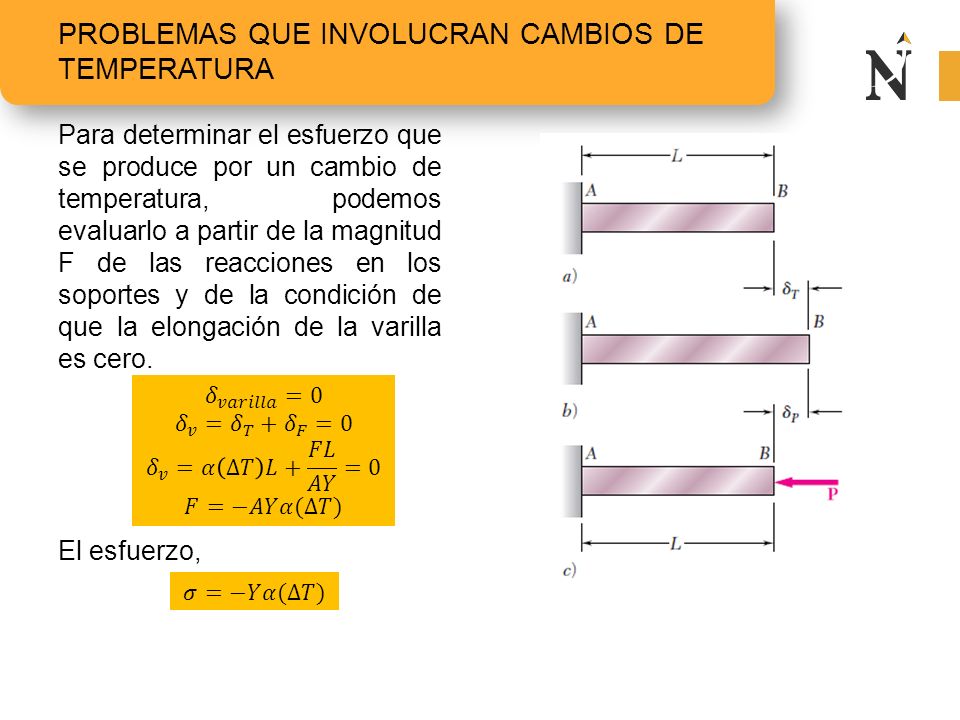
Los problemas que involucran cambios de temperatura tratan sobre calcular la temperatura final de un objeto después de que gana o pierde calor. Este calor puede ser absorbido (aumentando la temperatura) o liberado (disminuyendo la temperatura).
La fórmula principal que usamos es: Q = m * c * ΔT
Donde:
- Q es la cantidad de calor transferido (medido en julios o calorías).
- m es la masa del objeto (medida en gramos o kilogramos).
- c es el calor específico del material. El calor específico es la cantidad de calor necesaria para elevar la temperatura de 1 gramo de sustancia en 1 grado Celsius (medido en J/g°C o cal/g°C).
- ΔT es el cambio de temperatura. Se calcula como la temperatura final (Tf) menos la temperatura inicial (Ti): ΔT = Tf - Ti.
Pasos para resolver problemas de cambios de temperatura:
- Identifica las variables conocidas: Lee el problema cuidadosamente y anota los valores de Q, m, c, Ti o Tf que se te dan.
- Determina la variable desconocida: ¿Qué es lo que te están pidiendo calcular? (Q, m, c, Ti o Tf).
- Usa la fórmula Q = m * c * ΔT: Si necesitas encontrar ΔT, puedes despejar la fórmula así: ΔT = Q / (m * c).
- Calcula ΔT: Sustituye los valores conocidos en la fórmula y realiza la operación.
- Calcula la temperatura final (Tf) o inicial (Ti): Si ya tienes ΔT, puedes usar ΔT = Tf - Ti para encontrar Tf (Tf = Ti + ΔT) o Ti (Ti = Tf - ΔT). Recuerda considerar el signo de ΔT. Si ΔT es positivo, la temperatura aumentó; si es negativo, disminuyó.
- Unidades: Asegúrate de usar las unidades correctas. Si la masa está en gramos, y el calor específico en J/g°C, entonces Q estará en Julios.
Ejemplo:
¿Cuánto calor se necesita para calentar 200 gramos de agua de 20°C a 50°C? El calor específico del agua es 4.186 J/g°C.
- m = 200 g
- c = 4.186 J/g°C
- Ti = 20°C
- Tf = 50°C
- ΔT = 50°C - 20°C = 30°C
- Q = ?
Usando la fórmula: Q = m * c * ΔT
Q = (200 g) * (4.186 J/g°C) * (30°C) = 25116 J
Por lo tanto, se necesitan 25116 Julios para calentar el agua.
Recuerda practicar con diferentes problemas para dominar este concepto. Presta atención a las unidades y al signo de ΔT.