Primer Nivel De La Molecula Del Agua
¡Hola a todos! Vamos a repasar la estructura molecular del agua para tu examen. No te preocupes, ¡lo haremos juntos!
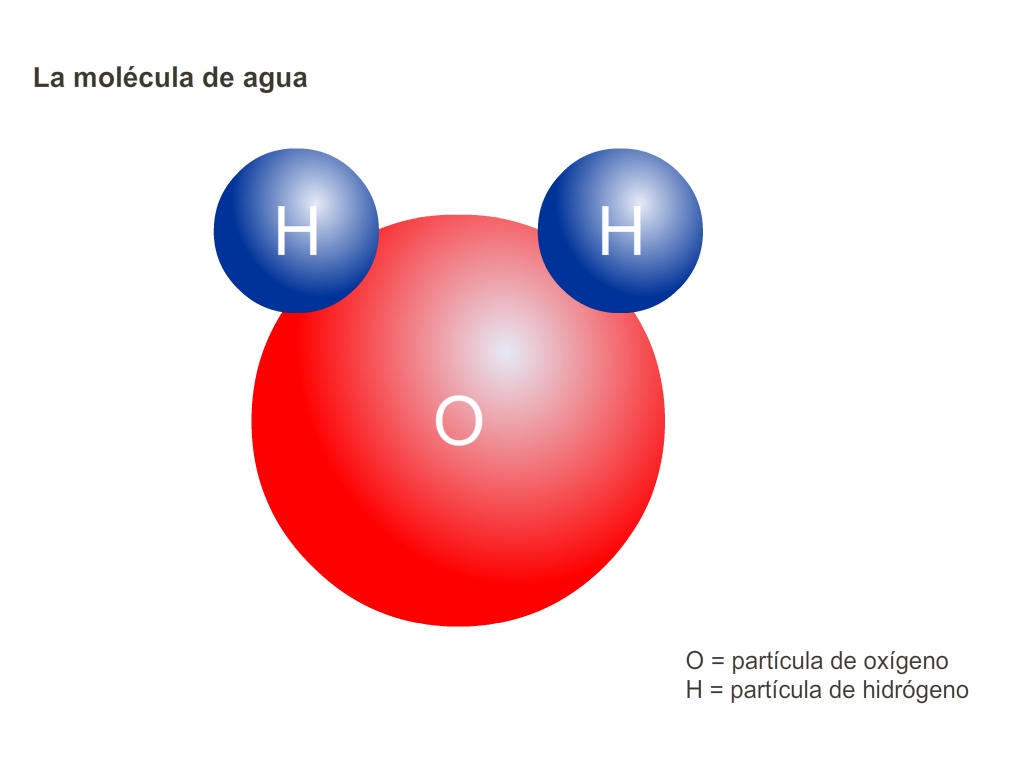
La Fórmula del Agua: H2O
El agua está representada por la fórmula H2O. Esto significa que una molécula de agua está formada por dos átomos de hidrógeno (H) y un átomo de oxígeno (O). Es la base de todo lo que veremos después.
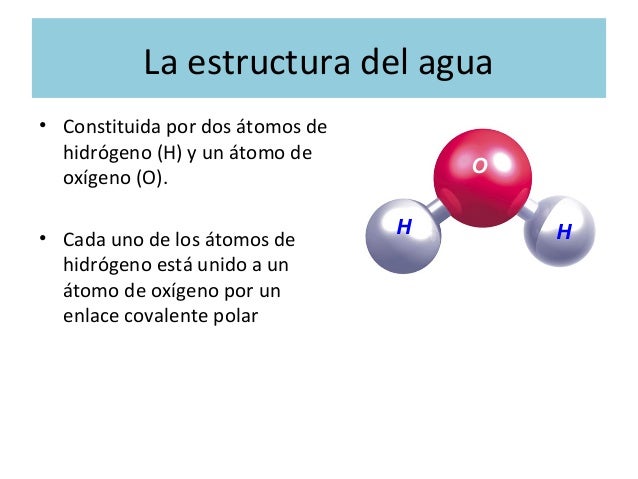
El Enlace Covalente
Los átomos de hidrógeno y oxígeno se unen mediante un enlace covalente. ¿Qué es esto? Es cuando los átomos *comparten* electrones. Este compartir electrones les permite alcanzar una configuración electrónica estable.
En el agua, el oxígeno comparte electrones con cada uno de los hidrógenos. Este compartir forma el enlace que los mantiene unidos. Recuerda, los enlaces covalentes son fuertes.
Electronegatividad y Polaridad
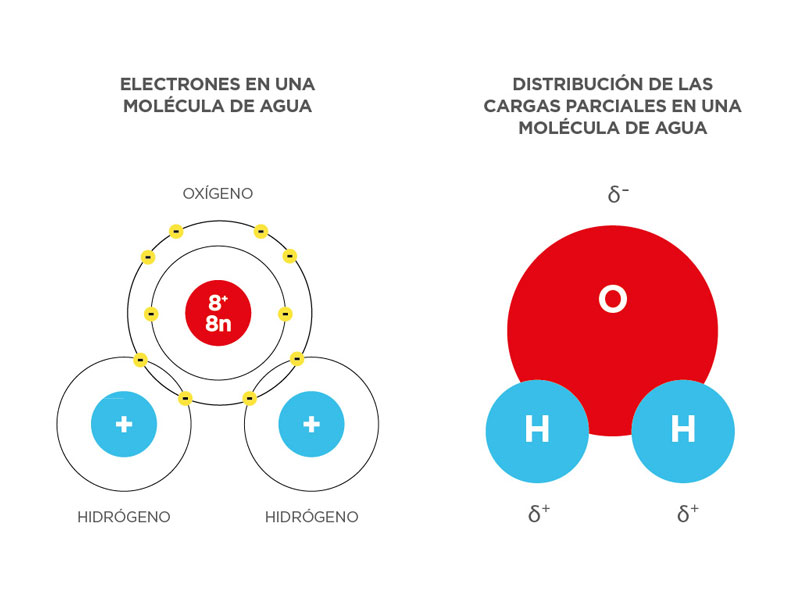
El oxígeno es más electronegativo que el hidrógeno. Esto significa que el oxígeno atrae los electrones compartidos con más fuerza. Esta diferencia en la atracción de electrones es crucial.
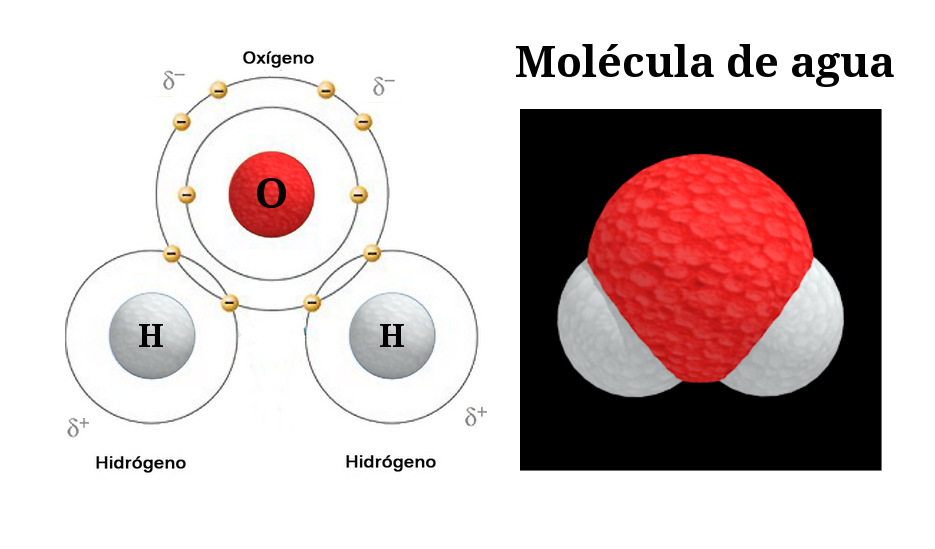
Debido a la mayor electronegatividad del oxígeno, la molécula de agua se vuelve polar. El oxígeno adquiere una carga parcialmente negativa (δ-) y los hidrógenos adquieren cargas parcialmente positivas (δ+). Piensa en ello como un imán pequeño con polos positivos y negativos.
La Geometría Molecular: Una Forma Curva
La molécula de agua *no* es lineal. Tiene una forma curva o angular. El ángulo entre los dos enlaces O-H es de aproximadamente 104.5 grados. Esta forma es muy importante.
La forma curva se debe a la repulsión entre los pares de electrones no enlazantes del oxígeno. Estos pares de electrones empujan los átomos de hidrógeno, resultando en la forma angular. La forma curva contribuye a las propiedades únicas del agua.
Enlaces de Hidrógeno
Debido a su polaridad, las moléculas de agua pueden formar enlaces de hidrógeno entre sí. El extremo positivo de una molécula de agua (el hidrógeno) es atraído por el extremo negativo de otra (el oxígeno).
Los enlaces de hidrógeno son mucho más débiles que los enlaces covalentes. Sin embargo, son cruciales para muchas de las propiedades especiales del agua. Piensa en los enlaces de hidrógeno como una fuerza de atracción entre moléculas de agua vecinas.
Propiedades Clave del Agua Derivadas de su Estructura
La estructura molecular del agua explica muchas de sus propiedades únicas. Por ejemplo, su alto calor específico. Esto significa que necesita mucha energía para cambiar su temperatura.
También explica su tensión superficial. La tensión superficial es la fuerza que permite a algunos insectos caminar sobre el agua. Y su capacidad como solvente universal para sustancias polares.
Resumen
Repasemos los puntos clave rápidamente:
- El agua es H2O.
- Tiene enlaces covalentes.
- Es una molécula polar debido a la electronegatividad del oxígeno.
- Su forma es curva o angular.
- Forma enlaces de hidrógeno entre moléculas.
- Su estructura molecular explica muchas de sus propiedades especiales.
¡Ya casi lo tienes! Repasa este material, haz algunos ejercicios de práctica y estarás listo para el examen. ¡Mucha suerte!