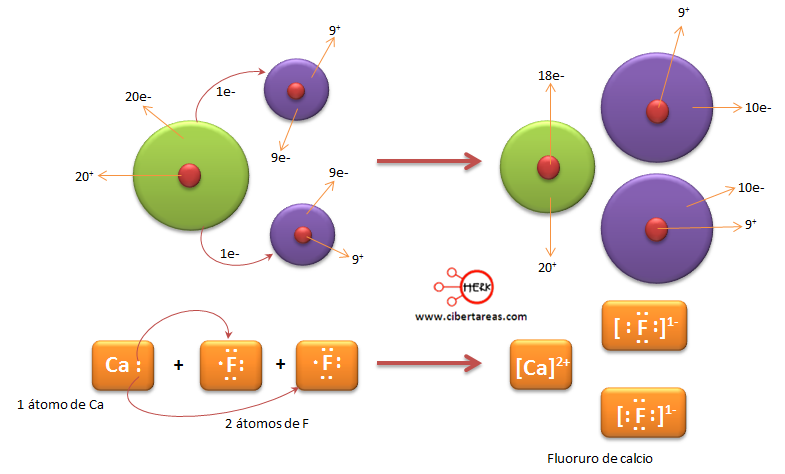
Observa La Estructura De Lewis Del Fluoruro De Calcio

Vamos a explorar la Estructura de Lewis del Fluoruro de Calcio (CaF2). En términos sencillos, la Estructura de Lewis muestra cómo se enlazan los átomos y sus electrones de valencia en una molécula o compuesto. El Fluoruro de Calcio es un compuesto iónico, lo que significa que está formado por la transferencia de electrones entre átomos.
Paso 1: Identificar los átomos y sus electrones de valencia
Primero, identifiquemos los átomos involucrados y cuántos electrones de valencia (los electrones en la capa más externa) tiene cada uno. El Calcio (Ca) está en el grupo 2 de la tabla periódica, por lo que tiene 2 electrones de valencia. El Flúor (F) está en el grupo 17 (halógenos) y tiene 7 electrones de valencia. Recuerda que el Fluoruro de Calcio tiene la fórmula CaF2, lo que significa que hay un átomo de Calcio y dos átomos de Flúor.
Paso 2: Transferencia de Electrones (Enlace Iónico)
El Calcio 'quiere' perder sus dos electrones de valencia para lograr una configuración electrónica estable (como un gas noble). El Flúor 'quiere' ganar un electrón para lograr también una configuración electrónica estable. Por lo tanto, el Calcio cede sus dos electrones. Cada átomo de Flúor acepta un electrón del Calcio.
Paso 3: Formación de Iones
Cuando el Calcio pierde dos electrones, se convierte en un ion positivo con una carga de +2 (Ca2+). Los iones positivos se llaman cationes. Cada átomo de Flúor, al ganar un electrón, se convierte en un ion negativo con una carga de -1 (F-). Los iones negativos se llaman aniones. Ahora tenemos un ion Calcio (Ca2+) y dos iones Fluoruro (F-).
Paso 4: Representación de la Estructura de Lewis
En la Estructura de Lewis del Fluoruro de Calcio, no se dibujan líneas que representen enlaces covalentes (compartir electrones). En su lugar, mostramos los iones formados.
Primero, escribimos el símbolo del Calcio (Ca) entre corchetes y le ponemos una carga de +2: [Ca]2+. Esto indica que ha perdido dos electrones. Como el Calcio perdió sus electrones, no dibujamos puntos alrededor de él.
Luego, escribimos el símbolo del Flúor (F) entre corchetes y le ponemos una carga de -1: [F]-. Dibujamos 8 puntos alrededor del Flúor. Estos 8 puntos representan los 7 electrones de valencia originales *más* el electrón que ganó del Calcio. Repetimos esto para el segundo ion Fluoruro: [F]- con 8 puntos a su alrededor.
La estructura completa sería algo similar a: [F]- [Ca]2+ [F]- (con 8 puntos alrededor de cada ion Fluoruro). Es importante notar que los corchetes y las cargas son cruciales para indicar que estamos representando iones.
Paso 5: Comprender la Atracción Electrostática
La fuerza que mantiene unidos a los iones en el Fluoruro de Calcio es la atracción electrostática entre las cargas opuestas (Ca2+ y F-). Esta es la característica principal de los enlaces iónicos. El Fluoruro de Calcio no forma moléculas discretas como el agua (H2O). En su lugar, forma una red cristalina donde cada ion Calcio está rodeado por iones Fluoruro y viceversa.
En resumen, la Estructura de Lewis del Fluoruro de Calcio muestra la transferencia de electrones del Calcio al Flúor, formando iones con cargas opuestas que se atraen entre sí, creando un compuesto iónico estable.
+Use+Lewis+dot+diagrams+to+determine+the+formula+of+calcium+fluoride..jpg)