Nomenclatura Tradicional De Los Hidruros Metalicos
¡Hola a todos! Hoy vamos a explorar la nomenclatura tradicional de los hidruros metálicos. Este tema es fundamental para comprender cómo nombramos y entendemos estos compuestos químicos. Prepárense para un viaje lleno de reglas y ejemplos.
¿Qué son los Hidruros Metálicos?
Un hidruro metálico es un compuesto químico binario. Esto significa que está formado por dos elementos. Estos elementos son un metal y el hidrógeno. El hidrógeno actúa con un estado de oxidación negativo (-1).
Es importante recordar que no todos los metales forman hidruros. Algunos metales de transición, por ejemplo, forman hidruros no estequiométricos. Pero, en general, los metales alcalinos y alcalinotérreos son los que forman hidruros más comunes.
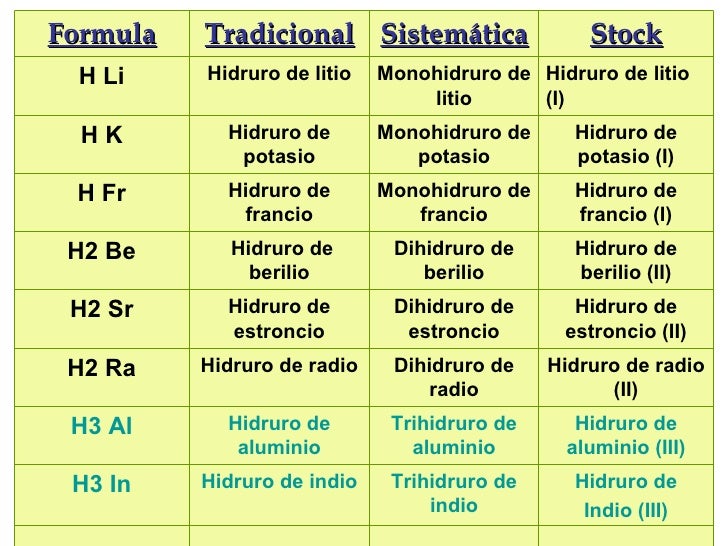
Nomenclatura Tradicional: Un Vistazo
La nomenclatura tradicional es un sistema antiguo. Se usa para nombrar compuestos químicos. En el caso de los hidruros metálicos, es bastante sencilla. Se basa en el nombre del metal y su estado de oxidación.
La regla general es: "Hidruro de" seguido del nombre del metal. Si el metal tiene un solo estado de oxidación, no se necesita más información. Si el metal tiene más de un estado de oxidación, se utilizan sufijos como "-oso" e "-ico".
Estados de Oxidación y Sufijos
Aquí es donde entran en juego los estados de oxidación. El estado de oxidación indica la carga eléctrica que tendría un átomo. Esto si todos los enlaces fueran iónicos.
Si un metal tiene dos estados de oxidación, el menor se indica con el sufijo "-oso". El mayor se indica con el sufijo "-ico". Por ejemplo, si un metal tiene estados de oxidación +2 y +3, el compuesto con +2 tendrá el sufijo "-oso". El compuesto con +3 tendrá el sufijo "-ico".
Ejemplos Prácticos
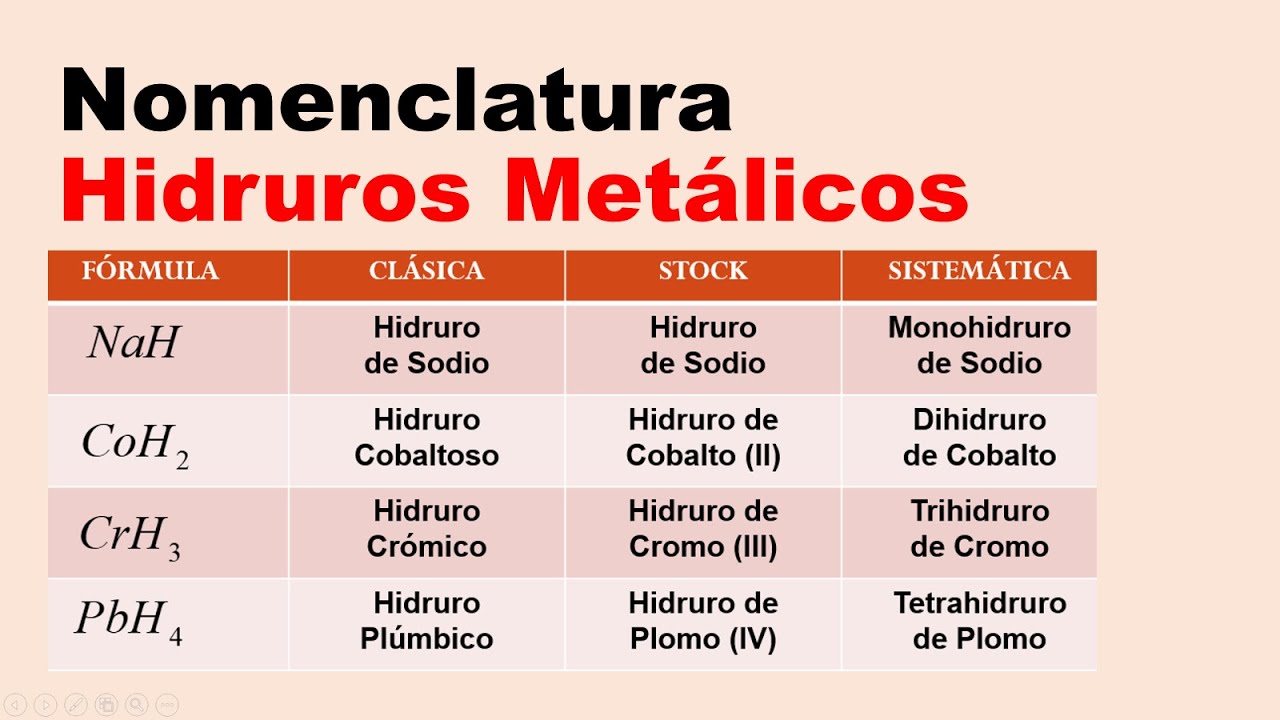
Veamos algunos ejemplos para aclarar las cosas. Consideremos el sodio (Na). El sodio tiene un único estado de oxidación: +1. Por lo tanto, el hidruro de sodio se llama simplemente Hidruro de Sodio (NaH). No necesitamos usar sufijos.
Ahora, veamos el caso del hierro (Fe). El hierro tiene dos estados de oxidación comunes: +2 y +3. El compuesto con hierro en estado de oxidación +2 se llama Hidruro Ferroso (FeH2). El compuesto con hierro en estado de oxidación +3 se llama Hidruro Férrico (FeH3).
Otro ejemplo: el cobre (Cu). El cobre tiene estados de oxidación +1 y +2. El hidruro con cobre +1 es el Hidruro Cuproso (CuH). El hidruro con cobre +2 es el Hidruro Cúprico (CuH2).
Aplicaciones Reales
Los hidruros metálicos tienen diversas aplicaciones. El Hidruro de Sodio (NaH) es un agente reductor muy fuerte en química orgánica. Se utiliza para sintetizar otros compuestos.
Otros hidruros metálicos, como el Hidruro de Litio y Aluminio (LiAlH4), también son importantes reductores. Se utilizan en la industria farmacéutica y en la investigación científica.
Algunos hidruros metálicos se utilizan como almacenadores de hidrógeno. Esto es importante para el desarrollo de tecnologías de energía limpia. Imagina coches que funcionen con hidrógeno almacenado en hidruros metálicos.
Resumen y Conclusión
La nomenclatura tradicional de los hidruros metálicos es un sistema simple. Nos permite nombrar estos compuestos de forma clara. Recuerda el uso de los sufijos "-oso" e "-ico" para diferenciar los estados de oxidación. Con práctica, nombrar hidruros metálicos será pan comido.
Espero que esta explicación haya sido útil. Recuerda que la práctica es clave para dominar la nomenclatura química. ¡Sigan explorando el fascinante mundo de la química!