Modelo Atomico De Sommerfeld Y Sus Postulados

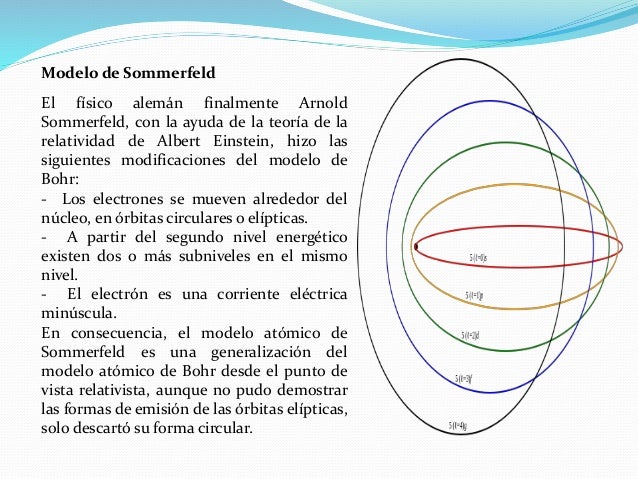
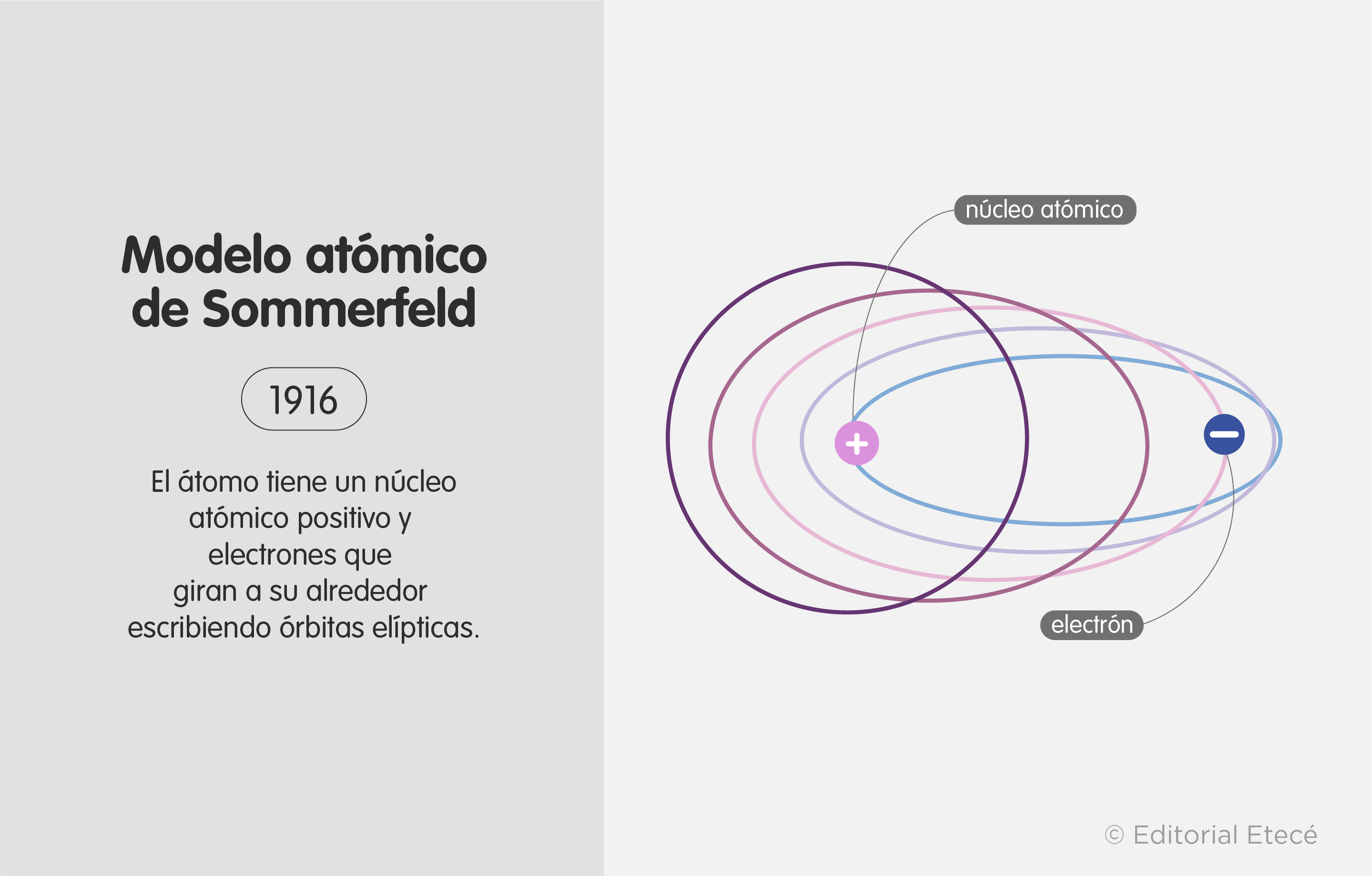
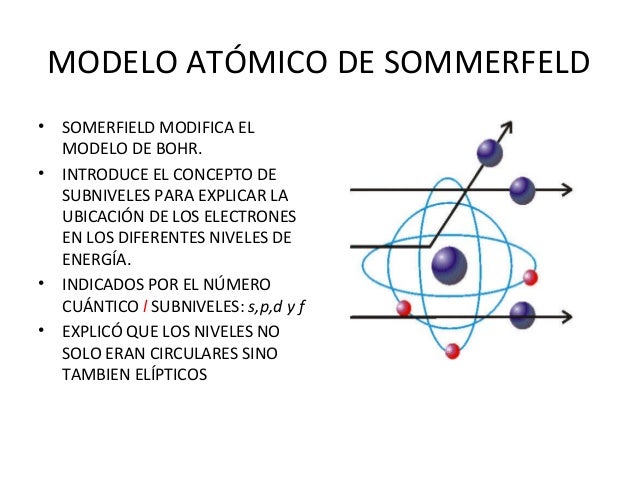
El Modelo Atómico de Sommerfeld es una mejora al modelo de Bohr. Bohr decía que los electrones giran en órbitas circulares alrededor del núcleo. Sommerfeld añadió algo más: ¡las órbitas no son solo circulares, también pueden ser elípticas!
¿Qué Postulados Incluyó Sommerfeld?
Sommerfeld, en esencia, hizo el modelo de Bohr más completo. Sus postulados principales son:
-
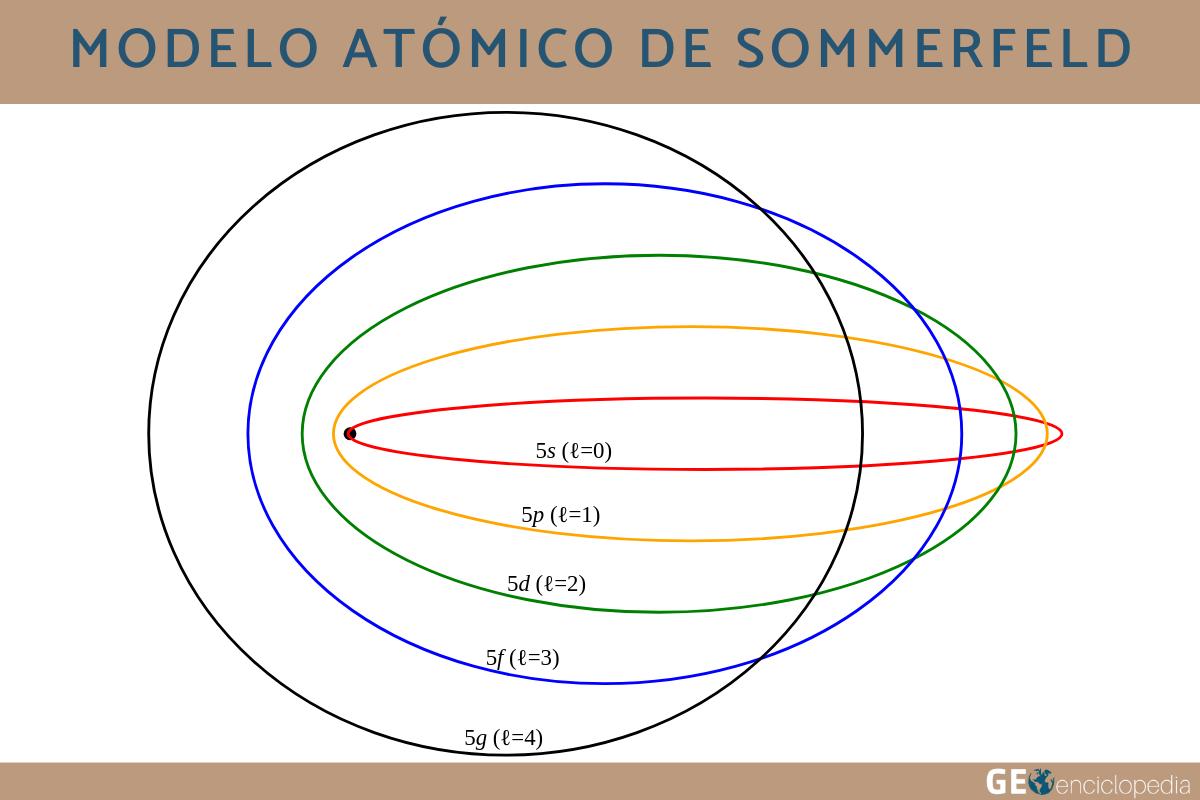
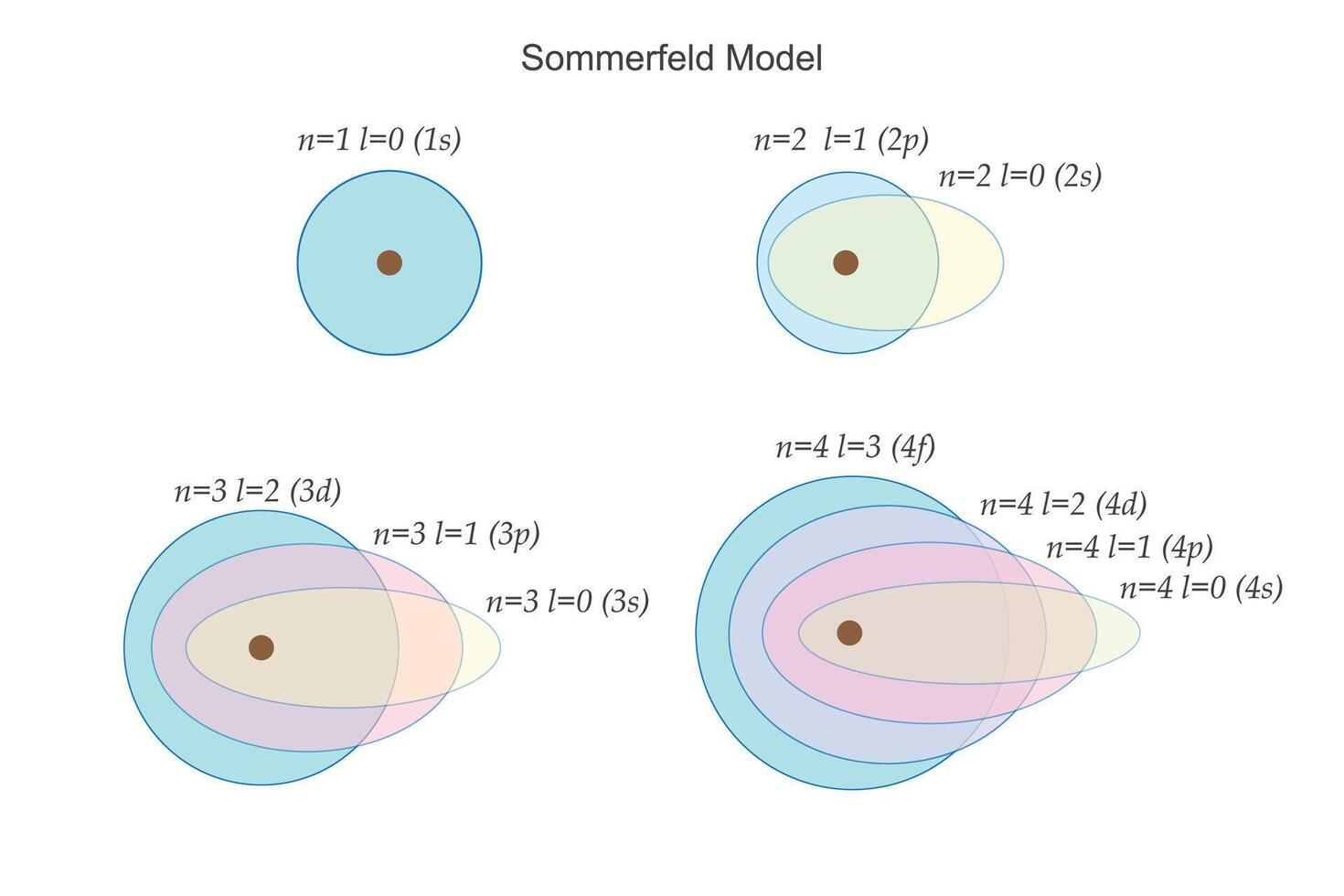
Órbitas Elípticas: Los electrones no solo giran en círculos. También pueden seguir caminos elípticos alrededor del núcleo. Imagina una canica moviéndose alrededor de una pelota de baloncesto. Puede dar vueltas en círculo, o en una forma ovalada. Así son las órbitas de Sommerfeld.
-
Número Cuántico Azimutal (l): Además del número cuántico principal (n) de Bohr, que indicaba el nivel de energía (ej: n=1, n=2, n=3), Sommerfeld introdujo el número cuántico azimutal (l). Este número define la forma de la órbita. Si l=0, la órbita es circular. Si l=1, l=2, etc., la órbita es elíptica. Piensa en "n" como el piso en un edificio, y "l" como el departamento en ese piso. Cada "departamento" (l) tiene una forma diferente.
-
Subniveles de Energía: Dentro de cada nivel de energía principal (n), hay subniveles de energía. Estos subniveles corresponden a las diferentes formas de las órbitas (elípticas o circulares). Volviendo al ejemplo del edificio, en cada piso (n) hay varios departamentos (l), y cada departamento tiene una energía ligeramente diferente.
-
Efectos Relativistas: Sommerfeld consideró los efectos relativistas de la velocidad del electrón. Es decir, a velocidades cercanas a la de la luz (aunque no tan cerca en el átomo, pero lo suficiente para hacer una diferencia), la masa del electrón aumenta, lo que afecta a la forma de la órbita. Esto es como un coche de carreras; a alta velocidad, el aire afecta su forma de moverse.
¿Por Qué Era Importante el Modelo de Sommerfeld?
El modelo de Sommerfeld fue un avance porque:
-
Explicaba el espectro de emisión de átomos más complejos: El modelo de Bohr funcionaba bien para el hidrógeno. Pero cuando se analizaban átomos con más electrones, aparecían líneas en el espectro que el modelo de Bohr no podía explicar. Sommerfeld, con sus órbitas elípticas y subniveles, pudo explicar esas líneas adicionales.
-
Introdujo la idea de que los electrones no solo tienen energía, sino también momento angular: El número cuántico azimutal (l) está relacionado con el momento angular del electrón, que es una medida de la "cantidad de giro" del electrón.
Limitaciones del Modelo de Sommerfeld
Aunque mejoró el modelo de Bohr, el modelo de Sommerfeld también tenía limitaciones. No podía explicar el efecto Zeeman (la división de las líneas espectrales bajo la influencia de un campo magnético) ni la intensidad relativa de las líneas espectrales. Además, seguía siendo un modelo que mezclaba ideas clásicas con ideas cuánticas, lo cual no era del todo consistente. Más tarde, la mecánica cuántica proporcionaría una descripción más precisa del átomo.
En resumen, el modelo atómico de Sommerfeld representó un paso importante en la comprensión de la estructura atómica, al introducir la idea de órbitas elípticas y subniveles de energía, lo que permitió explicar fenómenos que el modelo de Bohr no podía. Aunque fue superado por modelos más avanzados, su contribución fue fundamental.