Los Factores Que Influyen En Una Reaccion Quimica

Una reacción química es un proceso donde unas sustancias (reactivos) se transforman en otras (productos). Varias cosas influyen en qué tan rápido o lento ocurre esta transformación. A continuación, veremos los factores más importantes.
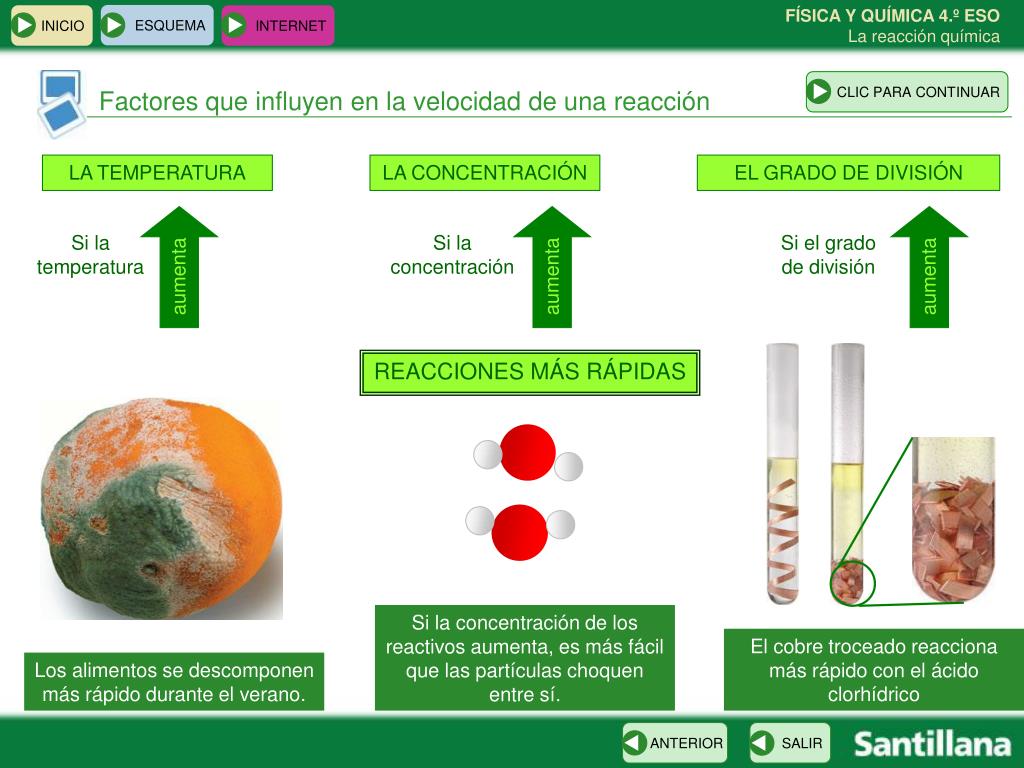
Concentración de los Reactivos
La concentración se refiere a la cantidad de reactivo presente en un espacio dado. Imagina una habitación llena de gente. Si hay más gente, es más probable que choquen entre sí. Lo mismo ocurre con las moléculas. Cuanto mayor sea la concentración de los reactivos, más choques habrá y, por lo tanto, más rápida será la reacción. Por ejemplo, encender un trozo de madera es más fácil con oxígeno puro (mayor concentración) que con aire (menor concentración de oxígeno).
Temperatura
La temperatura mide la energía de movimiento de las moléculas. Al aumentar la temperatura, las moléculas se mueven más rápido y chocan con más fuerza y frecuencia. Esto hace que la reacción se acelere. Piensa en cocinar: la comida se cocina más rápido a fuego alto (mayor temperatura). Una reacción lenta a temperatura ambiente puede ser muy rápida al calentarla.
Presencia de un Catalizador
Un catalizador es una sustancia que acelera una reacción química sin consumirse en el proceso. Actúa proporcionando una ruta de reacción alternativa que requiere menos energía. Es como un atajo en un camino largo. Por ejemplo, en los coches, los convertidores catalíticos usan catalizadores para reducir la contaminación. Sin el catalizador, la reacción sería mucho más lenta y contaminante.
Superficie de Contacto
La superficie de contacto es el área donde los reactivos pueden interactuar. Si un reactivo es sólido, dividirlo en trozos más pequeños aumenta su superficie de contacto. Imagina quemar un tronco grande versus astillas de madera. Las astillas se queman más rápido porque tienen más superficie expuesta al oxígeno. A mayor superficie de contacto, más rápida será la reacción.
Naturaleza de los Reactivos
La naturaleza de los reactivos se refiere a sus propiedades químicas intrínsecas. Algunas sustancias reaccionan más fácilmente que otras debido a su estructura atómica y electrónica. Por ejemplo, algunos metales reaccionan violentamente con el agua, mientras que otros apenas reaccionan. Esta diferencia se debe a la facilidad con la que sus átomos pueden perder o ganar electrones.
Presión (para Gases)
Para reacciones que involucran gases, la presión puede afectar la velocidad de la reacción. Al aumentar la presión, las moléculas de gas se acercan más entre sí, aumentando la frecuencia de los choques. Esto acelera la reacción. Es similar al efecto de la concentración, pero aplicado a gases. Por ejemplo, ciertas reacciones industriales que involucran gases se realizan a alta presión para aumentar la producción.
En resumen, la velocidad de una reacción química depende de la concentración, la temperatura, la presencia de un catalizador, la superficie de contacto, la naturaleza de los reactivos y, para gases, la presión. Comprender estos factores es clave para controlar y optimizar las reacciones químicas en diversos campos, desde la cocina hasta la industria.