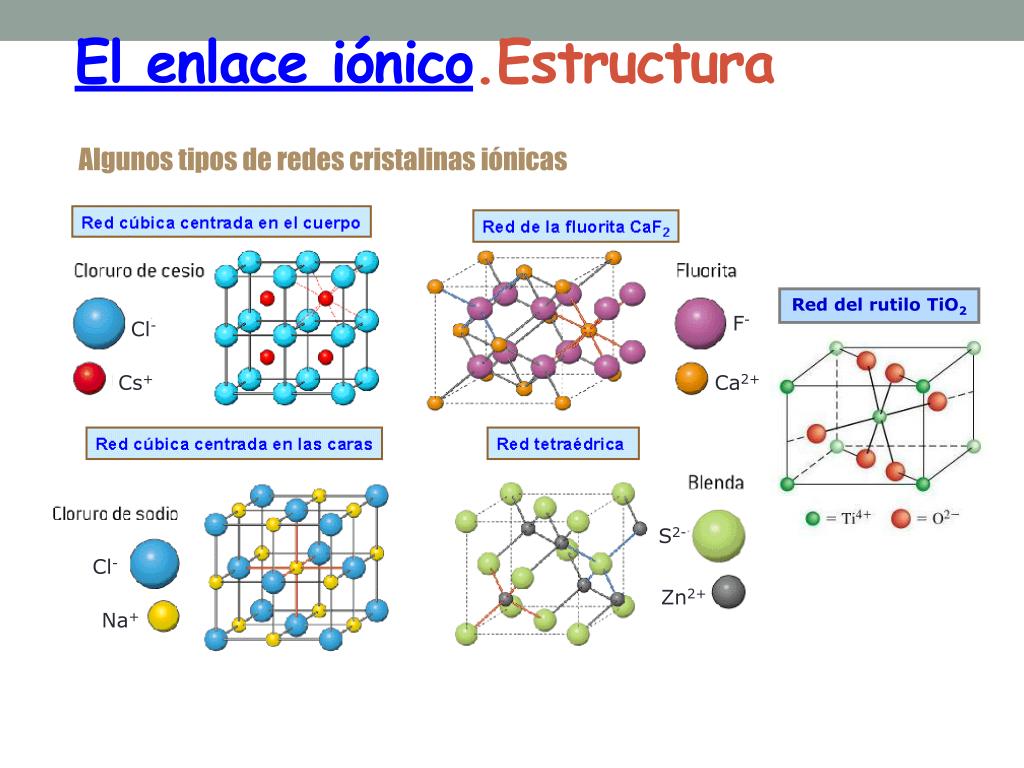
Los Compuestos Ionicos Forman Redes Cristalinas

Un compuesto iónico se forma cuando los átomos ganan o pierden electrones. Esto crea iones, que son átomos con carga eléctrica. Estos iones no andan solos. Se atraen entre sí debido a sus cargas opuestas, como imanes.
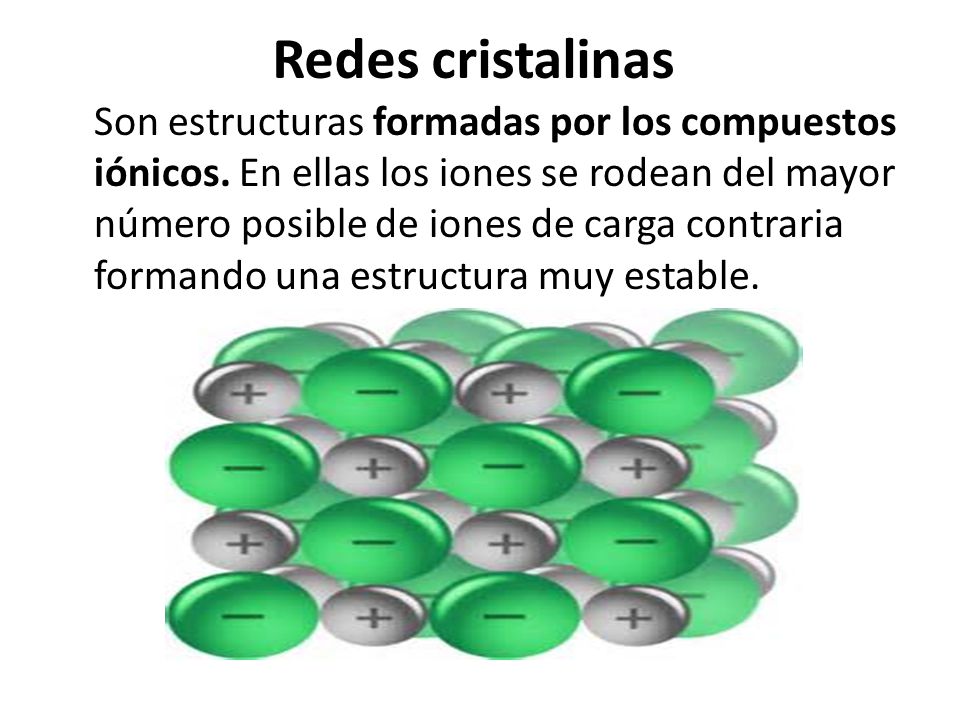
¿Qué es una red cristalina?
La red cristalina es la forma en que los iones se organizan en un compuesto iónico. Imagina un Lego. Cada pieza (ión) tiene un lugar específico y encaja con otras piezas para formar una estructura sólida. La red cristalina es esa estructura sólida, ordenada y repetitiva.
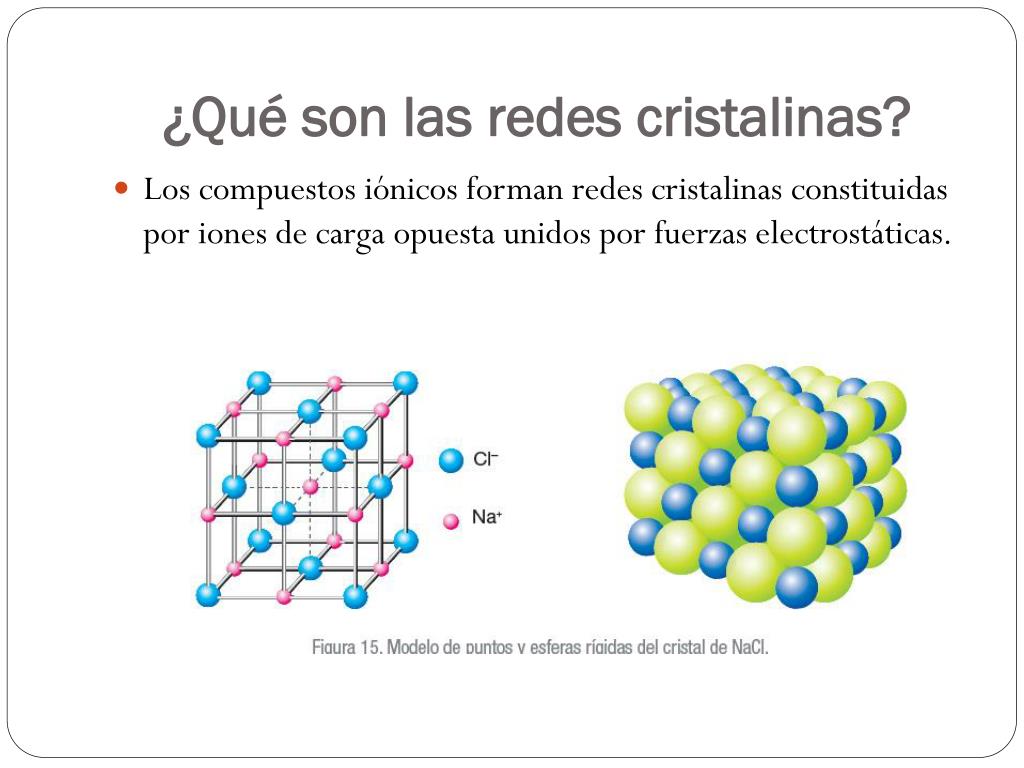
Definición simple: Una red cristalina es una estructura tridimensional organizada de iones con carga opuesta unidos por fuerzas electrostáticas.
¿Cómo se forma la red cristalina?
Los iones positivos (cationes) y los iones negativos (aniones) se atraen. Esta atracción es muy fuerte. En lugar de unirse de manera aleatoria, se organizan de la forma más eficiente posible. Eficiente significa que la atracción entre las cargas opuestas es máxima, y la repulsión entre las cargas iguales es mínima.
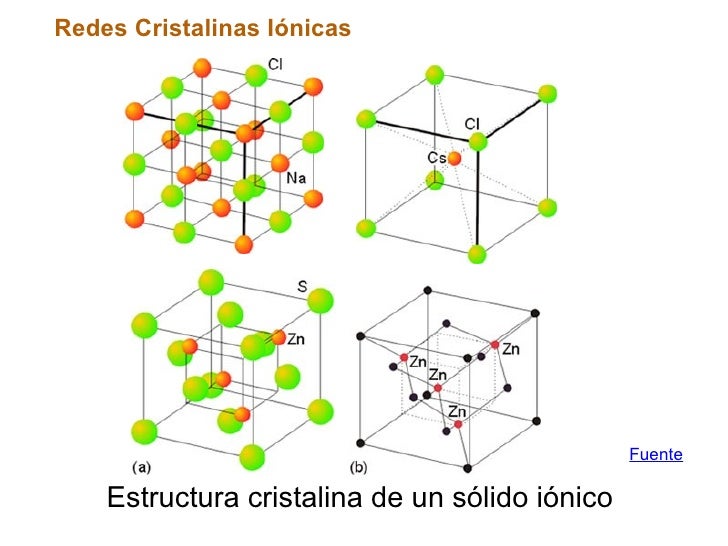
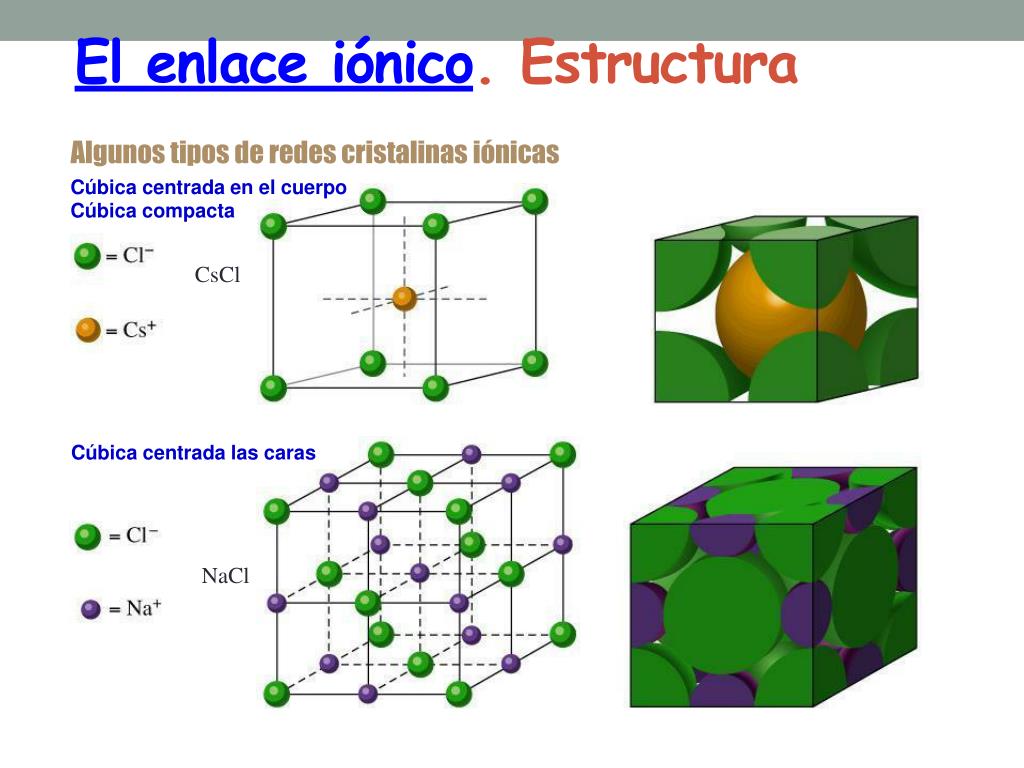
Piensa en el cloruro de sodio (sal de mesa), NaCl. El sodio (Na) pierde un electrón y se convierte en un catión (Na+). El cloro (Cl) gana un electrón y se convierte en un anión (Cl-). Los iones Na+ y Cl- se atraen. Se organizan en una red cúbica, donde cada ion Na+ está rodeado por seis iones Cl-, y viceversa.
Características de las redes cristalinas
- Alta estabilidad: La fuerte atracción entre los iones hace que las redes cristalinas sean muy estables y difíciles de romper. Por eso la sal de mesa es un sólido a temperatura ambiente.
- Altos puntos de fusión y ebullición: Se necesita mucha energía (calor) para superar la fuerte atracción entre los iones y romper la red. Por eso, los compuestos iónicos generalmente tienen altos puntos de fusión y ebullición.
- Dureza: Las redes cristalinas son duras debido a su estructura rígida. Sin embargo, también son quebradizas. Si aplicas suficiente fuerza, puedes romper la estructura de manera que los iones del mismo signo queden uno al lado del otro, generando repulsión y fractura.
- Conductividad eléctrica (en solución o fundidos): Los compuestos iónicos no conducen electricidad en estado sólido porque los iones están fijos en la red cristalina. Pero cuando se disuelven en agua o se funden, los iones se liberan y pueden moverse, permitiendo el flujo de corriente eléctrica.
Ejemplos de compuestos iónicos y sus redes cristalinas
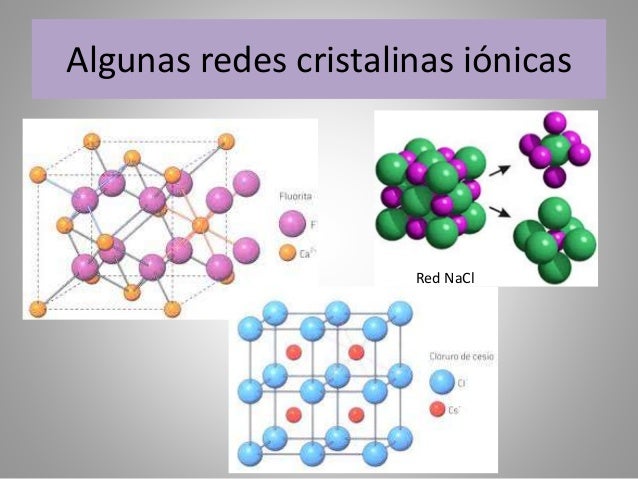
- Cloruro de sodio (NaCl): Sal de mesa. Red cúbica.
- Óxido de magnesio (MgO): Se usa en refractarios y antiácidos. Red cúbica.
- Fluoruro de calcio (CaF2): Se usa en la producción de ácido fluorhídrico. Red de fluorita.
En resumen, la formación de redes cristalinas es fundamental para las propiedades de los compuestos iónicos. La fuerte atracción entre los iones crea estructuras estables, duras y con altos puntos de fusión. La manera en que se organizan los iones dentro de la red cristalina influye directamente en el comportamiento del compuesto.
Recuerda: Las cargas opuestas se atraen, y esa atracción forma las redes cristalinas que dan a los compuestos iónicos sus características únicas.