Las Fuerzas De Dispersión De London
¡Hola estudiantes de química! Hoy vamos a explorar las Fuerzas de Dispersión de London, también conocidas como fuerzas de Van der Waals. Son fuerzas intermoleculares muy importantes. Piensa en ellas como pequeños imanes temporales que permiten que las moléculas se atraigan entre sí.
Imagina un grupo de canicas. Están todas amontonadas al azar. Las Fuerzas de London son como una ligera atracción gravitatoria entre esas canicas, haciendo que se mantengan un poco más juntas de lo que lo harían si no hubiera nada entre ellas.
¿Qué son las Fuerzas de Dispersión de London?
Las Fuerzas de London son atracciones débiles. Ocurren entre todas las moléculas, sean polares o no polares. Son causadas por fluctuaciones aleatorias en la distribución de electrones.
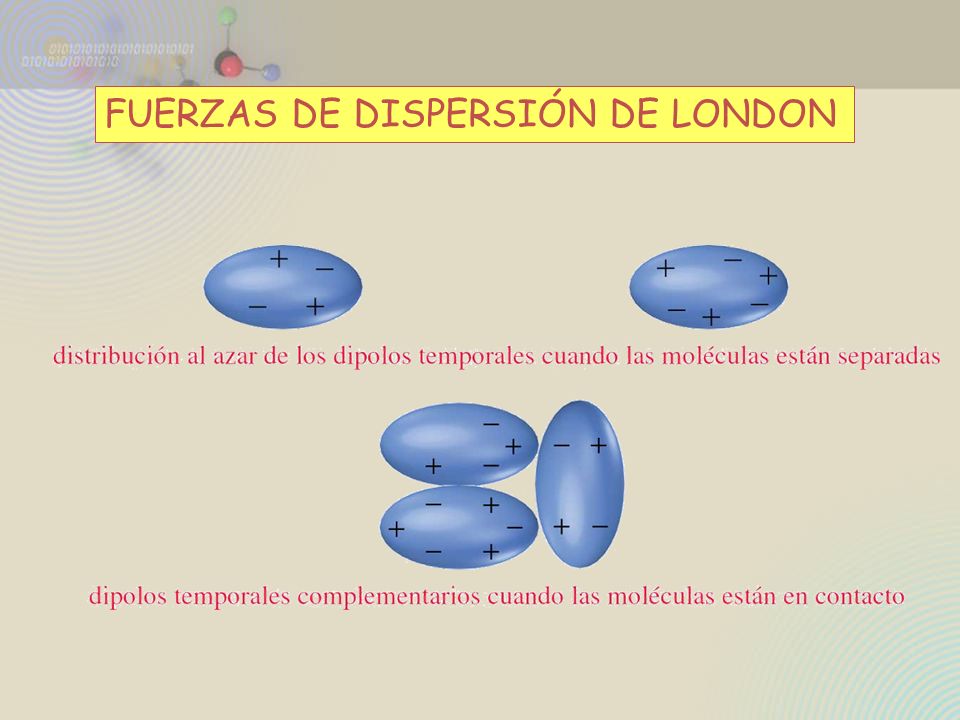
Piensa en una nube de electrones alrededor de un átomo. Normalmente, esta nube está distribuida uniformemente. Pero, por un instante, puede que haya más electrones en un lado del átomo que en el otro. Esto crea un dipolo temporal.
Imagina un globo. Normalmente, la carga está distribuida uniformemente. Pero si frotas una parte del globo contra tu cabello, esa parte se carga negativamente. La parte opuesta se carga positivamente. Eso es un dipolo temporal.
¿Cómo funcionan?
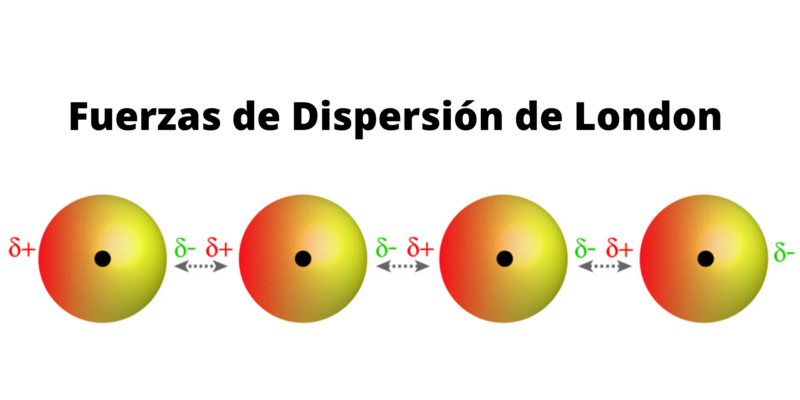
Este dipolo temporal induce un dipolo similar en un átomo vecino. Es como acercar un imán a un trozo de metal. El imán induce una polaridad en el metal.
Ahora tienes dos dipolos muy pequeños. Uno es temporal, el otro inducido. Estos dipolos se atraen entre sí. Esta atracción es la Fuerza de Dispersión de London.
Piensa en dos barcos flotando cerca uno del otro. Si un barco se inclina ligeramente hacia un lado, puede afectar la forma en que el agua se mueve alrededor del otro barco. Podría incluso tirar del otro barco hacia él. Las Fuerzas de London funcionan de manera similar.
Factores que afectan la fuerza de London
La fuerza de las Fuerzas de London depende de dos cosas principales: el tamaño de la molécula y su forma. Cuanto más grande sea la molécula, más electrones tendrá. Esto significa que puede formar dipolos temporales más grandes y más fuertes.
Imagina dos imanes: uno pequeño y uno grande. El imán grande tiene una fuerza de atracción mayor. Lo mismo ocurre con las moléculas y las Fuerzas de London.
La forma de la molécula también importa. Las moléculas con una mayor superficie tienen más contacto con otras moléculas. Esto significa que pueden formar más interacciones de London. Las moléculas largas y delgadas tienen una mayor superficie de contacto que las moléculas esféricas.
Piensa en dos hojas de papel. Una está arrugada en una bola. La otra está plana. La hoja plana tiene más superficie de contacto.
Ejemplos en la vida real
Las Fuerzas de London son responsables de que sustancias no polares como el metano (CH4) y el nitrógeno (N2) puedan existir en estado líquido o sólido a bajas temperaturas.
Considera el gecko, una lagartija que puede trepar paredes lisas. Los pies del gecko están cubiertos de millones de pelos diminutos. Estos pelos crean una gran superficie de contacto con la pared. Las Fuerzas de London entre las moléculas de los pelos y las moléculas de la pared son lo suficientemente fuertes como para sostener el peso del gecko.
El punto de ebullición de los alcanos aumenta con el número de carbonos. Esto se debe a que las moléculas más grandes tienen Fuerzas de London más fuertes. Por ejemplo, el metano (CH4) es un gas a temperatura ambiente, mientras que el octano (C8H18), un componente de la gasolina, es un líquido.
En resumen, las Fuerzas de Dispersión de London son atracciones débiles, pero importantes. Ocurren entre todas las moléculas y son causadas por fluctuaciones aleatorias en la distribución de electrones. La fuerza de estas fuerzas depende del tamaño y la forma de la molécula.