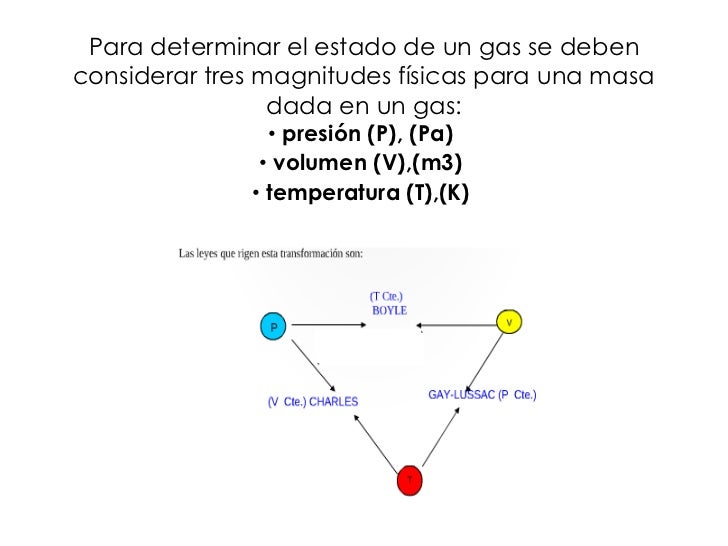
La Ley General Del Estado Gaseoso
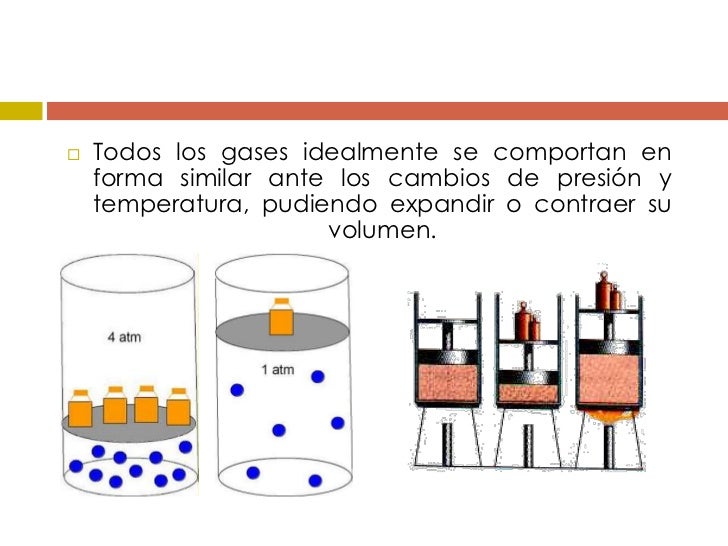
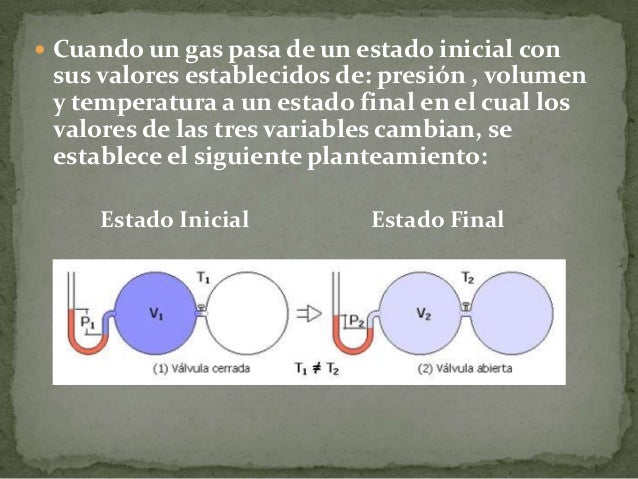
La Ley General del Estado Gaseoso describe la relación entre la presión, el volumen, la temperatura y la cantidad de un gas. Combina las leyes de Boyle, Charles, Gay-Lussac y Avogadro.
Esta ley se expresa matemáticamente como: PV = nRT. Donde P es la presión, V es el volumen, n es el número de moles, R es la constante de los gases ideales y T es la temperatura.
Aquí te explico cómo usarla paso a paso.
Paso 1: Identifica las variables
Primero, lee cuidadosamente el problema. Identifica qué variables te dan y cuál debes encontrar. Las variables comunes son: la Presión (P), usualmente en atmósferas (atm), Pascales (Pa) o mmHg. El Volumen (V), usualmente en litros (L) o metros cúbicos (m³). El Número de moles (n), en moles (mol). La Temperatura (T), siempre en Kelvin (K). La Constante de los gases ideales (R), que tiene un valor de 0.0821 L·atm/mol·K si usas atmósferas y litros.
Paso 2: Convierte las unidades (si es necesario)
Asegúrate de que todas las unidades sean consistentes. La temperatura debe estar siempre en Kelvin. Para convertir de Celsius a Kelvin, usa la fórmula: K = °C + 273.15. Por ejemplo, si te dan 25°C, entonces T = 25 + 273.15 = 298.15 K. Si el volumen está en mililitros (mL), divídelo entre 1000 para obtener litros (L).
Paso 3: Escribe la ecuación
Escribe la Ley General del Estado Gaseoso: PV = nRT. Esta es tu fórmula base. Asegúrate de tenerla a la mano.
Paso 4: Despeja la variable que buscas
Dependiendo de lo que te pidan, debes despejar la variable correspondiente. Por ejemplo, si quieres encontrar la presión (P), divide ambos lados de la ecuación por V: P = nRT / V. Si quieres encontrar el volumen (V), divide ambos lados de la ecuación por P: V = nRT / P. Si quieres encontrar el número de moles (n), divide ambos lados de la ecuación por RT: n = PV / RT. Si quieres encontrar la temperatura (T), divide ambos lados de la ecuación por nR: T = PV / nR.
Paso 5: Sustituye los valores y calcula
Una vez que tengas la ecuación despejada, sustituye los valores de las variables que conoces. Asegúrate de incluir las unidades. Por ejemplo, si tienes n = 2 moles, R = 0.0821 L·atm/mol·K, T = 300 K y V = 10 L, y quieres encontrar la presión, usarías: P = (2 mol * 0.0821 L·atm/mol·K * 300 K) / 10 L. Calcula el resultado. En este caso, P = 4.926 atm.
Paso 6: Verifica tu respuesta
Asegúrate de que tu respuesta tenga sentido. Considera las unidades. Si calculaste la presión, tu respuesta debe estar en unidades de presión (atm, Pa, mmHg). Si calculaste el volumen, tu respuesta debe estar en unidades de volumen (L, m³). Revisa tus cálculos para evitar errores.
Ejemplo:
Un gas ocupa un volumen de 5 L a una temperatura de 27°C y una presión de 2 atm. ¿Cuántos moles de gas hay?
Paso 1: P = 2 atm, V = 5 L, T = 27°C. Queremos encontrar n.
Paso 2: T = 27 + 273.15 = 300.15 K.
Paso 3: PV = nRT
Paso 4: n = PV / RT
Paso 5: n = (2 atm * 5 L) / (0.0821 L·atm/mol·K * 300.15 K) = 0.406 moles.
Paso 6: La respuesta tiene sentido y está en moles.