Imagenes De Modelo Atomico De Bohr
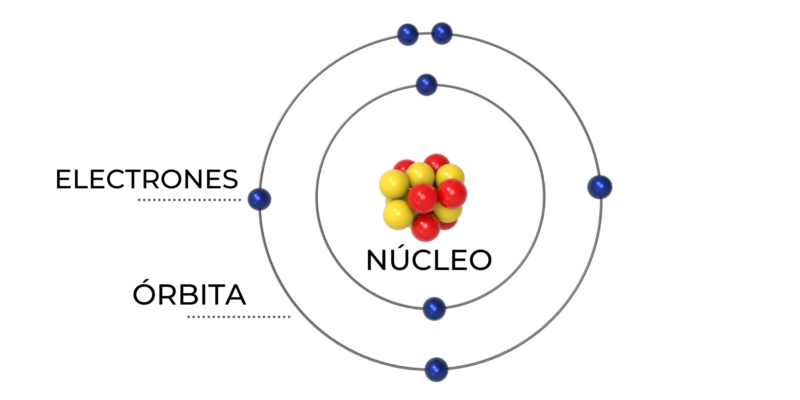
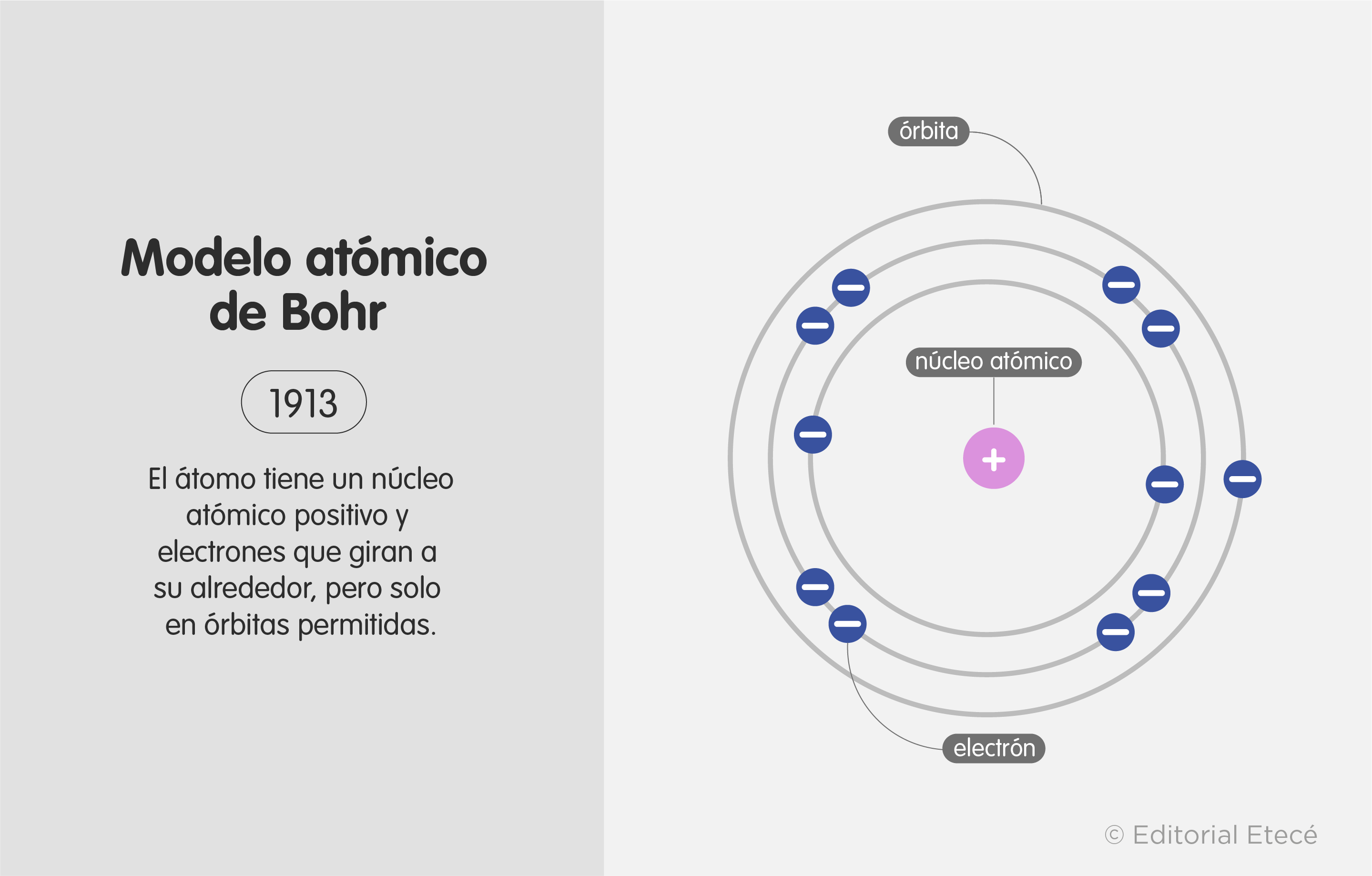
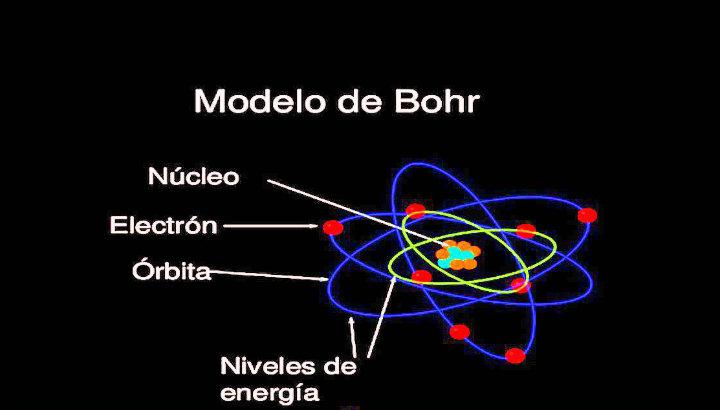
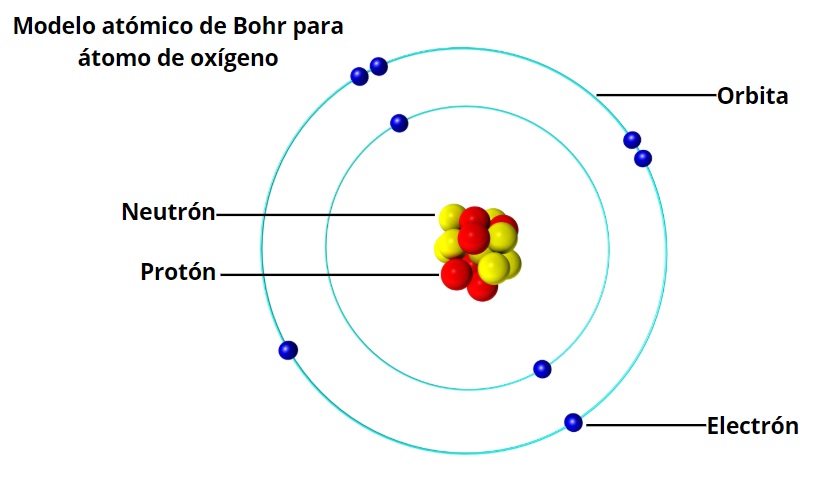
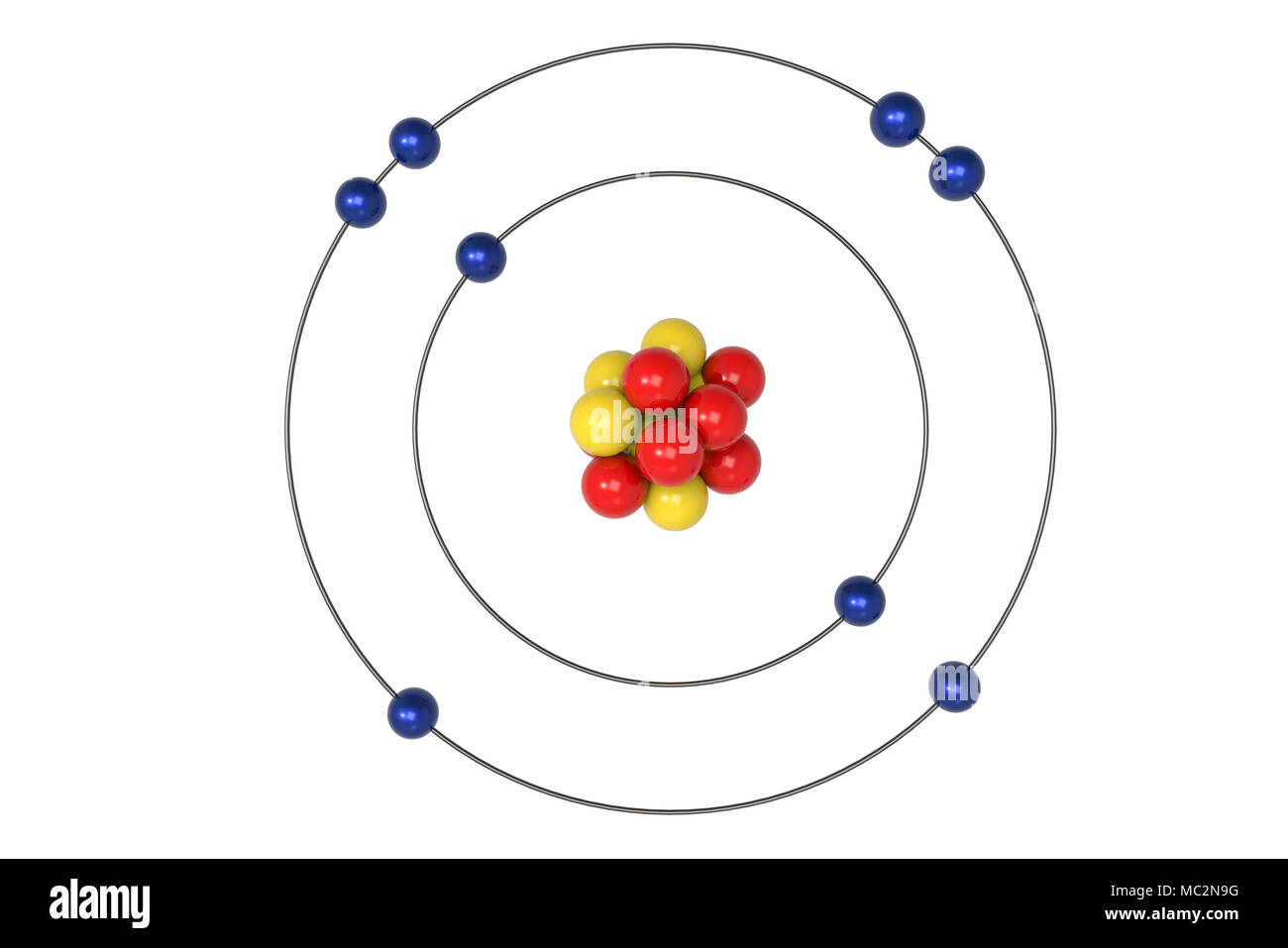
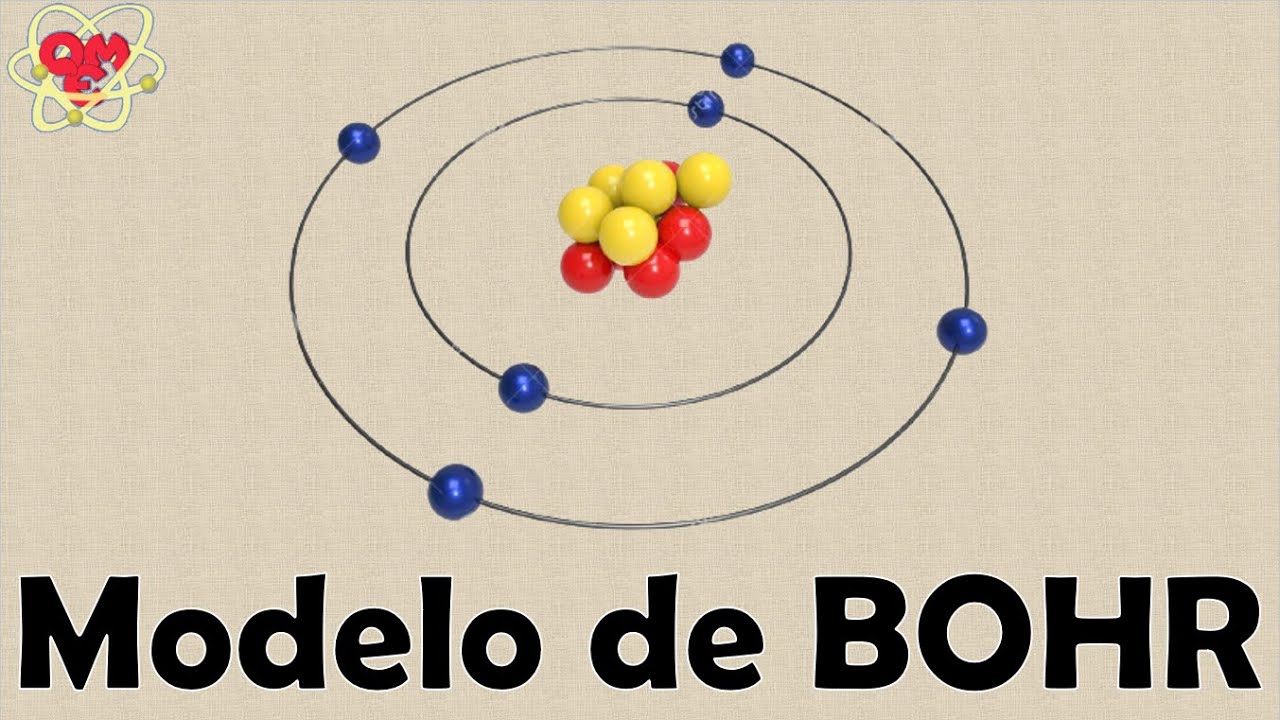
El Modelo Atómico de Bohr, propuesto por Niels Bohr en 1913, representa una mejora significativa sobre modelos atómicos previos. Postula que los electrones orbitan el núcleo en niveles de energía específicos, como planetas alrededor del sol. A diferencia de la visión clásica, donde los electrones podrían orbitar a cualquier distancia, el modelo de Bohr establece que solo ciertas órbitas están permitidas, cada una correspondiente a un nivel de energía cuantificado.
Un aspecto clave del modelo es la cuantización de la energía. Esto significa que los electrones solo pueden ocupar órbitas con energías discretas. Cuando un electrón absorbe energía (por ejemplo, de un fotón), puede saltar a una órbita de mayor energía, un proceso llamado excitación. Cuando un electrón regresa a una órbita de menor energía, emite energía en forma de un fotón con una energía específica, explicando así los espectros de emisión atómica.
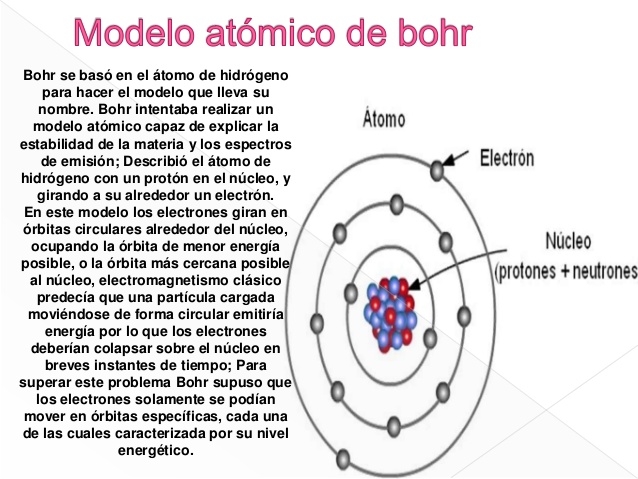
La estabilidad del átomo es otro pilar del modelo. Antes de Bohr, se pensaba que los electrones al orbitar el núcleo radiarían energía continuamente, espiralizando hacia el núcleo y causando el colapso del átomo. Bohr postuló que los electrones en órbitas permitidas no radian energía, manteniendo la estabilidad atómica a menos que sufran una transición entre niveles de energía.
El modelo introduce el concepto de números cuánticos, aunque de forma simplificada. Cada órbita se caracteriza por un número cuántico principal (n = 1, 2, 3, ...), que determina la energía del electrón en esa órbita. Cuanto mayor sea el valor de n, mayor será la energía y la distancia promedio del electrón al núcleo.
Un ejemplo simple es el átomo de hidrógeno, que tiene un solo protón y un solo electrón. El electrón puede ocupar diferentes niveles de energía, y las transiciones entre estos niveles dan lugar a las líneas espectrales características del hidrógeno. Otro ejemplo es el átomo de helio ionizado (He+), que también tiene un solo electrón y puede ser descrito con precisión por el modelo de Bohr.
A pesar de sus limitaciones al tratar átomos más complejos con múltiples electrones, el modelo de Bohr fue fundamental para el desarrollo de la mecánica cuántica. Su concepto de cuantización de la energía y órbitas específicas de los electrones sentó las bases para la comprensión moderna de la estructura atómica y el comportamiento de la materia. Su principal aplicación reside en su valor histórico y su rol como precursor de la teoría cuántica, ayudando a entender inicialmente los espectros atómicos y la estabilidad de la materia.

.jpg)