En Qué Consiste La Segunda Ley De La Termodinámica
Primero, entendamos la pregunta. Nos piden describir la Segunda Ley de la Termodinámica. Debemos explicar su significado central y sus implicaciones.
Recopilación de Información
Revisemos nuestros conocimientos previos. Busquemos fuentes confiables sobre termodinámica. Consideremos libros de texto, artículos científicos y recursos educativos en línea.
Identifiquemos los conceptos clave. Comprendamos entropía, procesos reversibles e irreversibles. Entendamos la dirección natural de los procesos termodinámicos.
Desarrollo de Posibles Soluciones
Consideremos varias formulaciones de la Segunda Ley. Pensemos en la imposibilidad de la eficiencia del 100% en motores térmicos. Consideremos la relación con el aumento de la entropía en sistemas aislados.
Construyamos una explicación clara y concisa. Evitemos jerga innecesaria. Utilicemos ejemplos para ilustrar los conceptos.
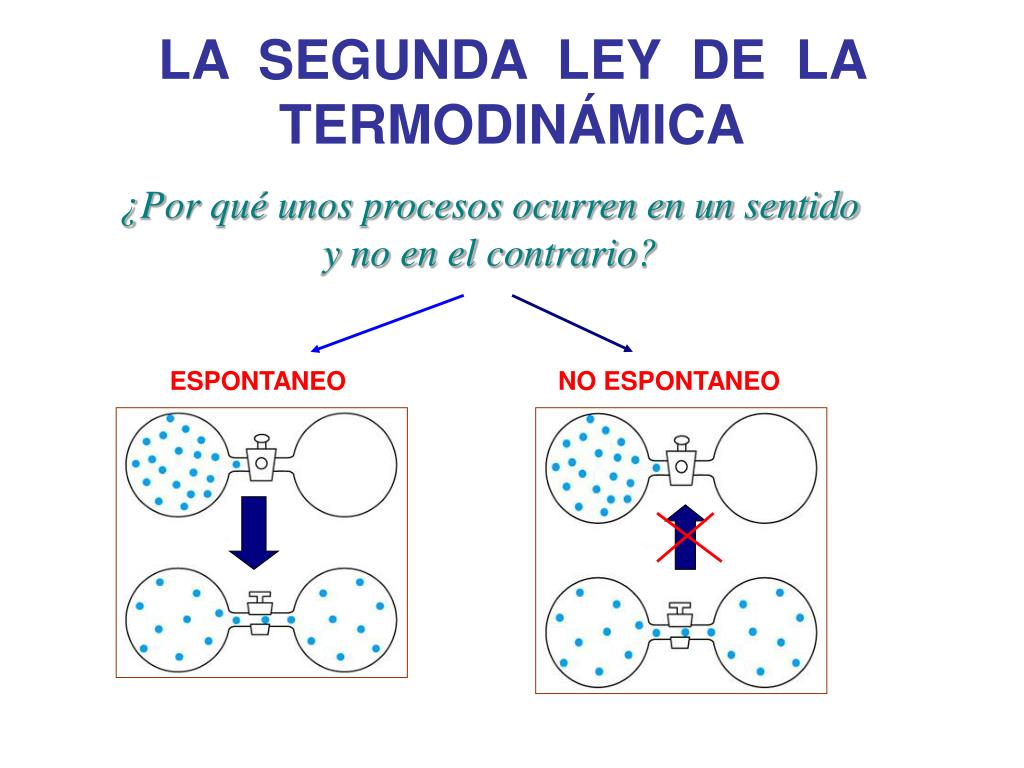
Presentemos la ley en términos de entropía. La entropía siempre aumenta en un sistema aislado. Presentemos la ley en términos de la dirección de los procesos. Los procesos espontáneos siempre van en una dirección determinada.
Estructura de la Respuesta
Comencemos con una definición general. Expliquemos la Segunda Ley en términos sencillos. Luego, profundicemos en detalles importantes.
Abordemos el concepto de entropía. Definamos entropía como una medida del desorden. Expliquemos cómo la entropía está relacionada con la Segunda Ley.
Analicemos los procesos reversibles e irreversibles. Describamos cómo la Segunda Ley afecta estos procesos. Los procesos reversibles son ideales y no ocurren en la realidad.
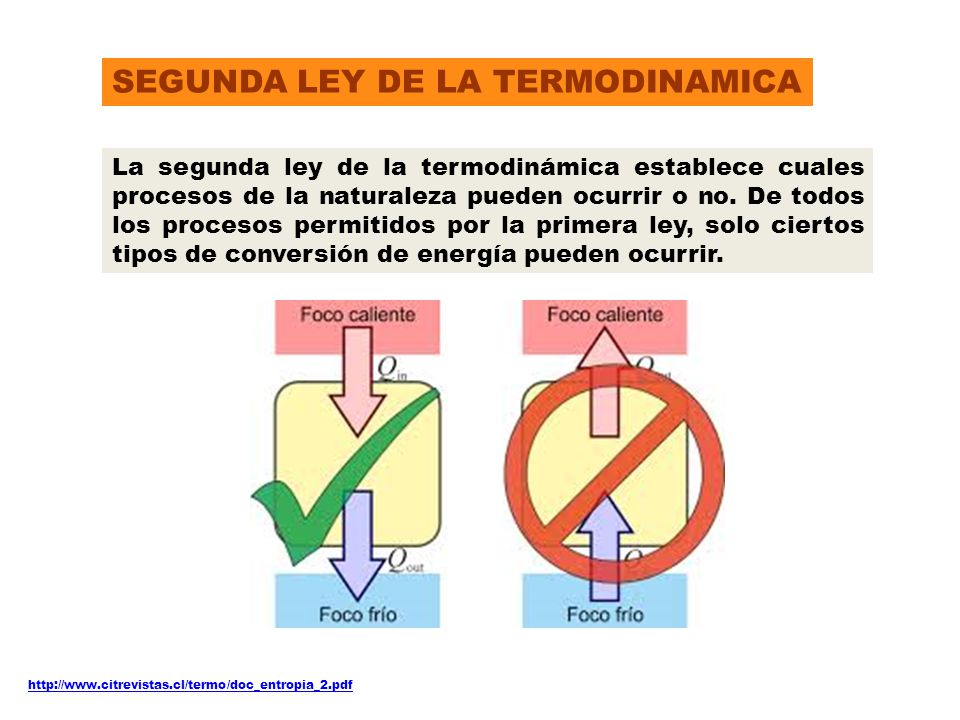
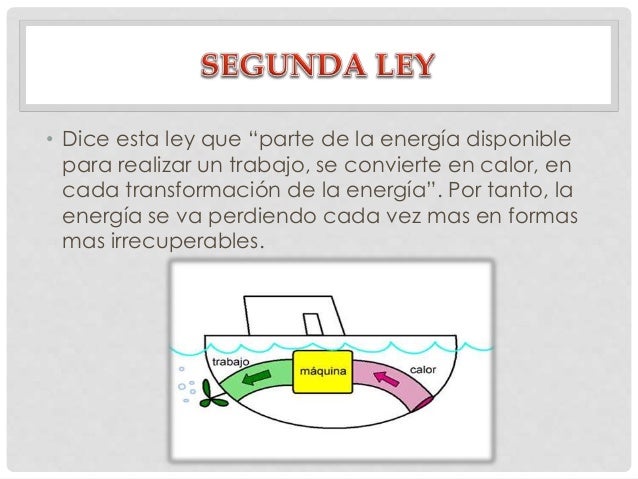
Expliquemos la imposibilidad de un motor térmico 100% eficiente. La Segunda Ley impone un límite en la eficiencia de los motores. Parte de la energía siempre se disipa como calor.
Incluyamos ejemplos prácticos. Pensemos en la expansión de un gas en un vacío. Pensemos en la transferencia de calor de un objeto caliente a uno frío.
Redacción de la Respuesta
Escribamos una respuesta clara y completa. Evitemos ambigüedades. Utilicemos un lenguaje preciso.
La Segunda Ley de la Termodinámica establece que la entropía total de un sistema aislado solo puede aumentar con el tiempo, o permanecer constante en procesos ideales donde el sistema está en equilibrio o experimenta un proceso reversible. En otras palabras, en cualquier proceso natural, siempre hay una tendencia hacia el aumento del desorden o la aleatoriedad en el universo.
La entropía, a menudo descrita como una medida del desorden o la aleatoriedad de un sistema, es el concepto central para comprender esta ley. Un sistema aislado tenderá espontáneamente a evolucionar hacia un estado de mayor entropía.
Además, la Segunda Ley implica que ningún motor térmico puede convertir toda la energía térmica en trabajo útil; siempre habrá una cierta cantidad de energía que se disipa como calor. Esto establece un límite fundamental a la eficiencia de cualquier dispositivo que convierta calor en trabajo.
Por ejemplo, cuando un gas se expande libremente en un vacío, el proceso es irreversible y la entropía del sistema aumenta. Otro ejemplo es la transferencia de calor de un objeto caliente a uno frío; el calor fluye naturalmente en esa dirección, aumentando la entropía total del sistema. Invertir este proceso requeriría trabajo externo.
La Segunda Ley de la Termodinámica es una de las leyes fundamentales de la física. Tiene profundas implicaciones en una amplia gama de campos, desde la ingeniería hasta la cosmología.
Verificación de la Respuesta
Revisemos la respuesta. Asegurémonos de que sea precisa y completa. Verifiquemos la gramática y la ortografía.
Comprobemos que la respuesta responde a la pregunta original. Asegurémonos de que la explicación sea clara y comprensible. Consideremos si la respuesta podría mejorarse.
Comparemos la respuesta con las fuentes originales. Asegurémonos de que no haya plagio. Asegurémonos de que la información sea correcta.