En Que Consiste La Regla Del Octeto

Analizar y resolver el problema de en qué consiste la Regla del Octeto implica comprender su fundamento y limitaciones. Buscaremos los átomos estables. Asumimos que la estabilidad atómica se rige por configuraciones electrónicas específicas.
Paso 1: Identificar el Concepto Clave
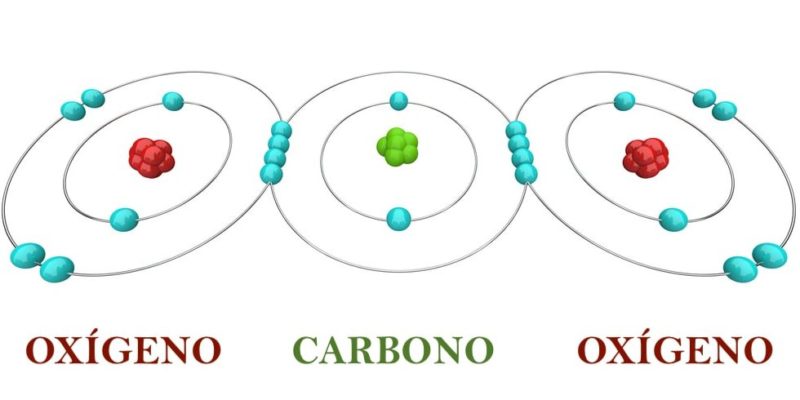
Primero, debemos precisar qué significa la Regla del Octeto. Esencialmente, postula que los átomos tienden a ganar, perder o compartir electrones. Lo hacen para alcanzar una configuración electrónica similar a la de un gas noble.
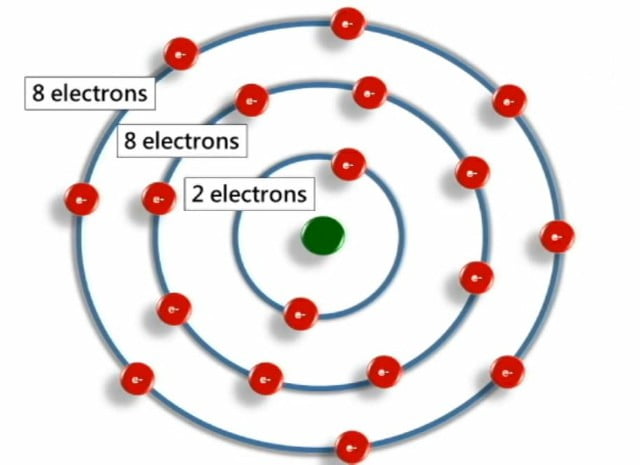
Esta configuración implica tener ocho electrones en su capa de valencia. Exceptuando el helio que busca tener dos. Esta es la meta que persiguen los átomos al enlazarse.
Paso 2: Desglosar la Definición
La capa de valencia es la capa electrónica más externa de un átomo. Es la que participa en la formación de enlaces químicos. Los electrones en esta capa son cruciales para las interacciones entre átomos.
Los gases nobles son un grupo de elementos (helio, neón, argón, kriptón, xenón y radón). Son excepcionalmente inertes y no reactivos. Esto se debe a su configuración electrónica estable.
El concepto de "ganar, perder o compartir electrones" se refiere a la formación de diferentes tipos de enlaces químicos. Enlace iónico, covalente y metálico son los principales.
Paso 3: Identificar las Asunciones Implícitas
La Regla del Octeto asume que todos los átomos buscan alcanzar una configuración de ocho electrones. Esto no siempre es cierto. Hay excepciones notables.
Se asume que la estabilidad se define únicamente por el número de electrones en la capa de valencia. Otros factores, como la carga nuclear efectiva, también influyen en la estabilidad.
Finalmente, se asume que los electrones se distribuyen uniformemente alrededor del núcleo. Esto ignora la naturaleza cuántica de los electrones y los orbitales atómicos.
Paso 4: Evaluar las Excepciones
El hidrógeno (H) busca tener dos electrones en su capa de valencia. El boro (B) a menudo es estable con seis electrones. El berilio (Be) puede ser estable con cuatro electrones.
Los átomos que pueden expandir su octeto incluyen elementos del tercer periodo en adelante. Estos pueden acomodar más de ocho electrones en su capa de valencia. Ejemplos incluyen el fósforo (P) y el azufre (S).
Las moléculas con un número impar de electrones no pueden cumplir la Regla del Octeto. El óxido nítrico (NO) es un ejemplo clásico.
Paso 5: Construir una Solución Integral
La Regla del Octeto es una herramienta útil para predecir la formación de enlaces químicos. Pero no es una ley universal.
Es importante considerar las excepciones y las limitaciones de la regla. Debemos recurrir a una comprensión más profunda de la estructura atómica y la teoría del enlace químico.
Para comprender la estabilidad atómica, debemos considerar factores como la carga nuclear efectiva, la energía de ionización y la afinidad electrónica. La Regla del Octeto es una simplificación útil, pero no la historia completa.
Paso 6: Conclusión
En conclusión, la Regla del Octeto es una guía valiosa. Describe la tendencia de los átomos a alcanzar configuraciones electrónicas estables. Pero presenta excepciones y simplificaciones.
Para analizar completamente un compuesto y su enlace, la regla debe contextualizarse. Así, reconocemos sus limitaciones y considerando otros factores relevantes.
Un análisis crítico de la Regla del Octeto nos permite aplicar el concepto de forma más efectiva. Entender sus límites profundiza nuestra comprensión de la química.