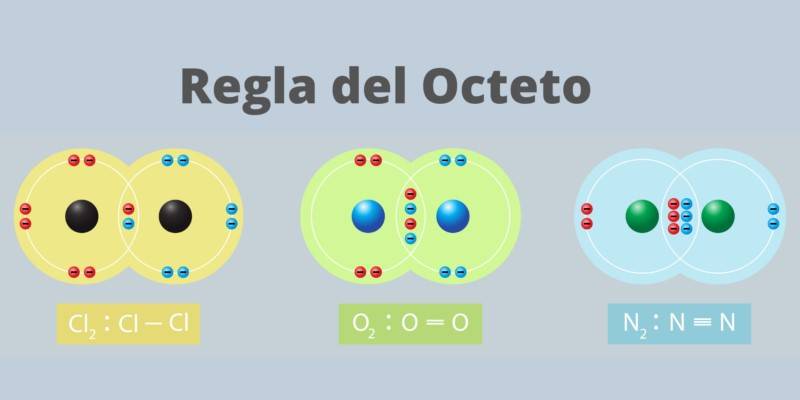
En Que Consiste La Regla Del Octeto Ejemplos

La regla del octeto es una regla básica en química. Dice que los átomos tienden a ganar, perder o compartir electrones para tener ocho electrones en su capa de valencia (la capa más externa).
¿Qué significa esto?
Imagina que los átomos son personas que quieren sentirse completos. Para sentirse completos, necesitan tener ocho "amigos" electrones rodeándolos en su "círculo social" (capa de valencia). Si no tienen ocho, intentarán conseguirlos.
Octeto significa "ocho". La regla del octeto busca que el átomo tenga ocho electrones.
La capa de valencia es la última capa de electrones de un átomo. Es la capa donde ocurren las reacciones químicas. Solo los electrones en esta capa participan en la formación de enlaces.
Cómo los átomos cumplen la regla del octeto
Los átomos pueden cumplir la regla del octeto de tres maneras:
- Ganando electrones: Si un átomo tiene, por ejemplo, siete electrones en su capa de valencia, "robará" un electrón a otro átomo para llegar a ocho.
- Perdiendo electrones: Si un átomo tiene, por ejemplo, un electrón en su capa de valencia, lo "regalará" a otro átomo para que su capa anterior (que ya tiene ocho electrones) se convierta en la capa de valencia.
- Compartiendo electrones: Dos átomos pueden "compartir" electrones para que ambos sientan que tienen ocho electrones en su capa de valencia. Esto forma un enlace covalente.
Ejemplos de la regla del octeto
Cloruro de Sodio (NaCl):
El sodio (Na) tiene un electrón en su capa de valencia. El cloro (Cl) tiene siete. El sodio *pierde* su electrón y se lo da al cloro. Ahora el sodio tiene ocho electrones en su capa anterior, y el cloro tiene ocho electrones en su capa de valencia. Se forman iones Na+ (positivo) y Cl- (negativo), que se atraen y forman el cloruro de sodio, la sal de mesa.
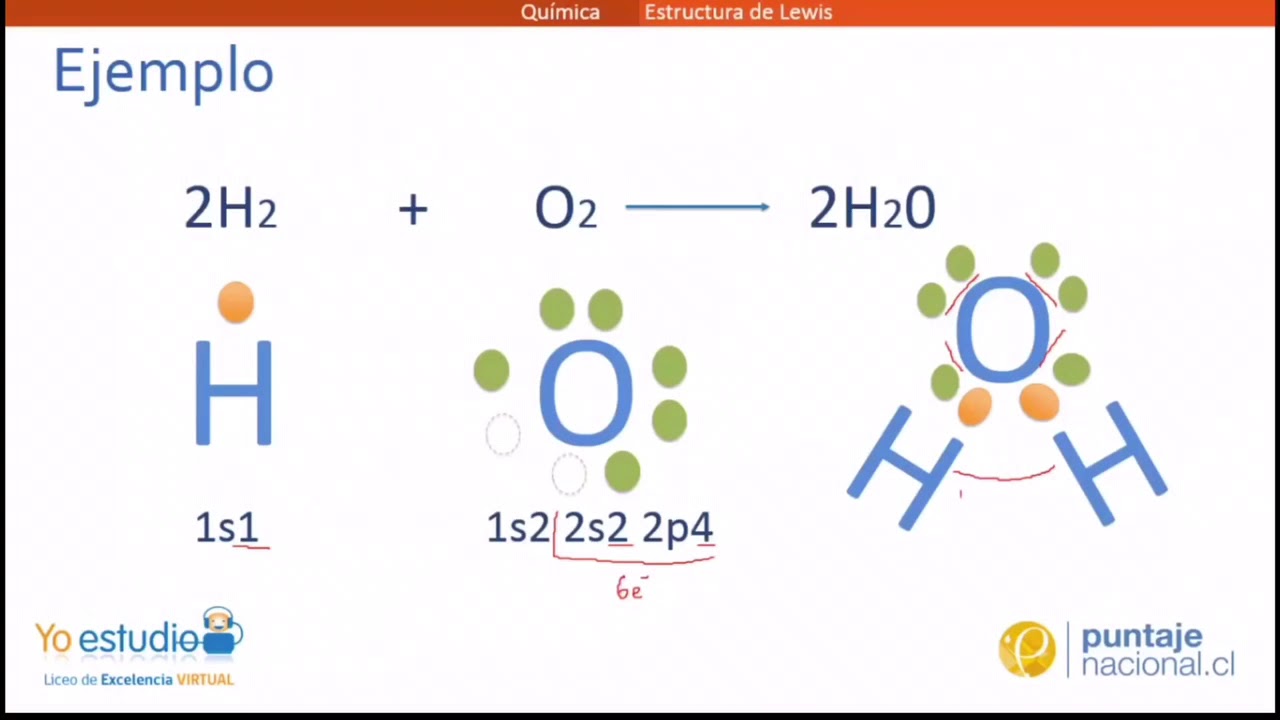
Agua (H2O):
El oxígeno (O) tiene seis electrones en su capa de valencia. El hidrógeno (H) tiene un electrón. Dos átomos de hidrógeno *comparten* sus electrones con el oxígeno. El oxígeno ahora "siente" que tiene ocho electrones (seis propios + dos compartidos). Cada hidrógeno "siente" que tiene dos electrones (uno propio + uno compartido). En este caso, el hidrógeno sigue la regla del dueto, que es similar a la del octeto pero para átomos pequeños como el hidrógeno, que solo necesita dos electrones para estar completo.
Metano (CH4):
El carbono (C) tiene cuatro electrones en su capa de valencia. El hidrógeno (H) tiene un electrón. Cuatro átomos de hidrógeno *comparten* cada uno su electrón con el carbono. El carbono ahora "siente" que tiene ocho electrones (cuatro propios + cuatro compartidos) y cada hidrógeno "siente" que tiene dos (uno propio + uno compartido).
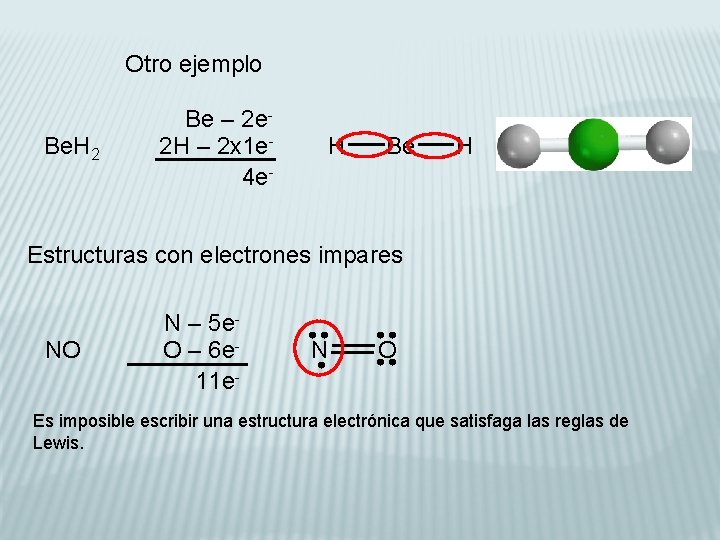
Excepciones a la regla del octeto
No todos los átomos siguen la regla del octeto perfectamente. Algunos átomos pueden tener menos de ocho electrones (como el berilio en el BeCl2) o más de ocho electrones (como el fósforo en el PCl5) en su capa de valencia. Sin embargo, la regla del octeto es una guía útil para entender cómo se forman los enlaces químicos.