En Qué Consiste El Enlace Covalente No Polar
Entendiendo el Problema
Primero, identifiquemos las palabras clave. Son *enlace covalente* y *no polar*. Es crucial comprender cada término individualmente. Luego, relacionaremos ambos conceptos.
¿Qué sabemos sobre los enlaces covalentes? ¿Qué implica la polaridad en un enlace? La combinación de estos conocimientos nos dará la respuesta. La polaridad influye directamente en la distribución electrónica.
Recopilación de Información Relevante
Investiguemos los enlaces covalentes. Son un tipo de enlace químico. Se forman por la compartición de electrones entre átomos. Estos átomos generalmente son no metales.
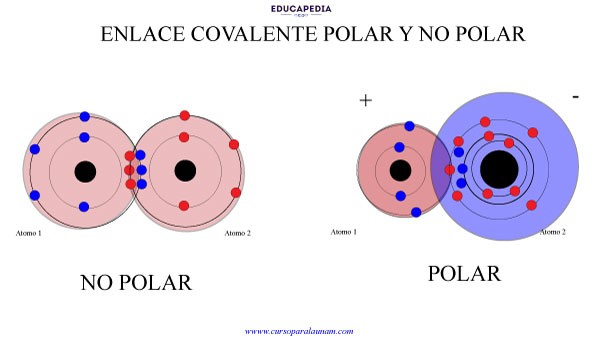
Investiguemos la polaridad. La polaridad describe la distribución desigual de electrones. Esta distribución desigual crea una carga parcial positiva (δ+) y una carga parcial negativa (δ-). La diferencia de *electronegatividad* entre los átomos es clave.
La *electronegatividad* mide la capacidad de un átomo para atraer electrones. Una gran diferencia de electronegatividad resulta en un enlace polar. Una diferencia pequeña o nula indica un enlace no polar. Esto es fundamental.
Desarrollo de Posibles Soluciones
Un enlace covalente no polar implica la compartición equitativa de electrones. Esto significa que no hay una acumulación significativa de carga en un átomo. Esto sugiere una pequeña o nula diferencia de electronegatividad.
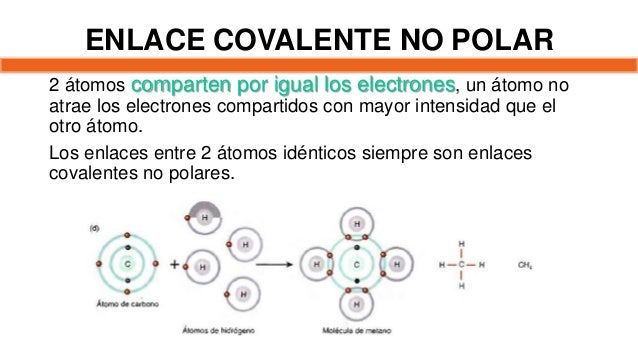
Consideremos átomos idénticos. Por ejemplo, dos átomos de hidrógeno (H₂). Su electronegatividad es la misma. Por lo tanto, comparten los electrones por igual.
¿Qué pasa con átomos diferentes? A pesar de ser diferentes, pueden tener electronegatividades similares. Esto también puede resultar en un enlace covalente no polar. Sin embargo, es menos común.
Verificación de la Respuesta Final
Definamos formalmente un enlace covalente no polar. Es un enlace químico formado por la compartición equitativa de electrones entre átomos. La diferencia de *electronegatividad* entre los átomos es mínima o inexistente.
Ejemplos comunes son los enlaces entre átomos del mismo elemento. Como el hidrógeno (H₂), el oxígeno (O₂), y el nitrógeno (N₂). También encontramos este tipo de enlace en moléculas orgánicas complejas.
Dentro de las moléculas orgánicas, los enlaces carbono-hidrógeno (C-H) se consideran no polares. Esto se debe a que el carbono y el hidrógeno tienen electronegatividades muy similares. Aunque existe una ligera diferencia, es insignificante. Por lo tanto, la distribución de electrones es casi equitativa.
Recordemos que la *polaridad* de un enlace influye en las propiedades de la molécula. Los enlaces no polares contribuyen a la hidrofobicidad. Por lo tanto, los enlaces no polares son importantes en la química orgánica y la bioquímica.
En resumen, un *enlace covalente no polar* es la compartición equitativa de electrones. Está caracterizado por una baja diferencia de electronegatividad. Esto resulta en una distribución uniforme de la carga eléctrica en la molécula.





.jpg)

