Ecuacion De Schrodinger Para El Atomo De Hidrogeno

La ecuación de Schrödinger para el átomo de hidrógeno es una piedra angular de la mecánica cuántica.
El Modelo Atómico Simplificado
El átomo de hidrógeno es el sistema atómico más simple. Solo contiene un protón y un electrón. Su simplicidad hace que sea un punto de partida ideal. Sirve para comprender átomos más complejos.
La Ecuación Independiente del Tiempo
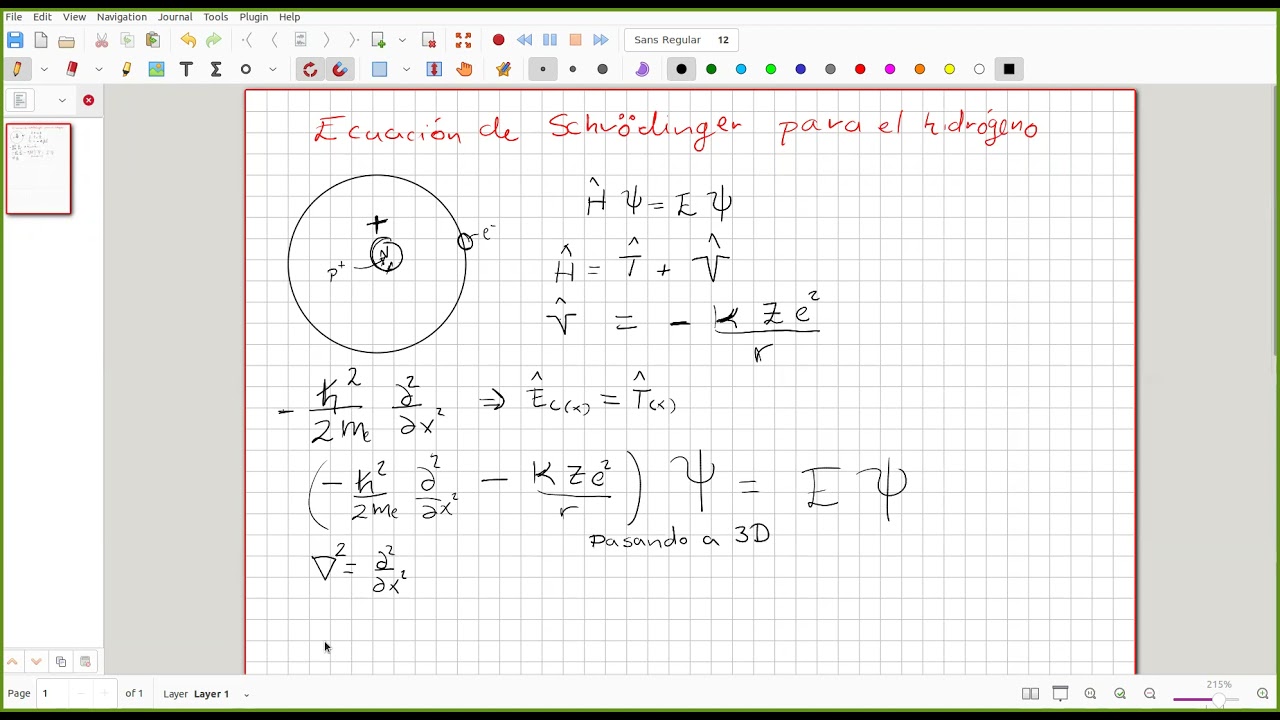
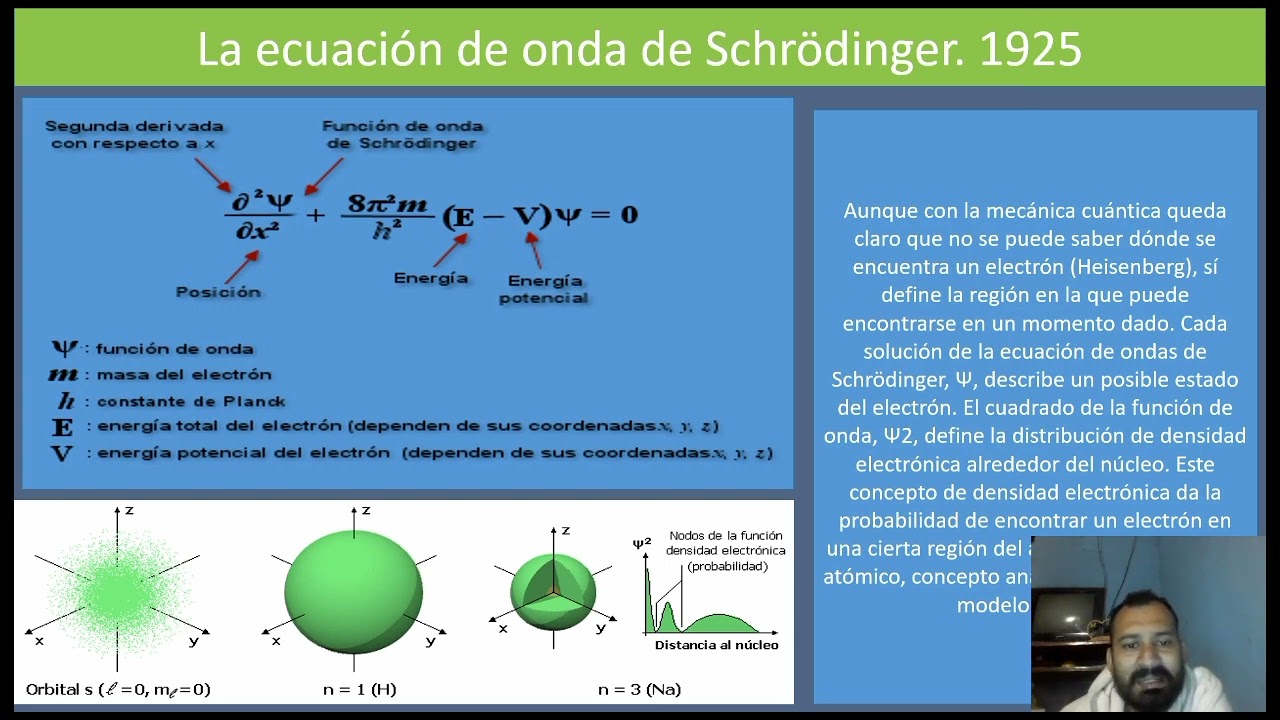
La ecuación de Schrödinger independiente del tiempo describe los estados estacionarios. Estos estados son de energía definida. Para el átomo de hidrógeno, se escribe: Hψ = Eψ. H es el operador hamiltoniano, ψ es la función de onda, y E es la energía.
El operador hamiltoniano incluye la energía cinética del electrón. También incluye la energía potencial debida a la atracción electrostática. La atracción es entre el electrón y el núcleo (protón).
Resolviendo la Ecuación
Resolver la ecuación de Schrödinger para el átomo de hidrógeno es complejo. Se utilizan coordenadas esféricas para aprovechar la simetría esférica. Esto transforma la ecuación en un conjunto de ecuaciones diferenciales más manejables.
Las soluciones se expresan en términos de funciones. Son las funciones radiales y los armónicos esféricos. Las funciones radiales dependen de la distancia al núcleo. Los armónicos esféricos describen la dependencia angular.
Números Cuánticos
Las soluciones están caracterizadas por números cuánticos. El número cuántico principal (n) determina la energía del electrón. El número cuántico del momento angular (l) determina la forma del orbital. El número cuántico magnético (ml) determina la orientación del orbital en el espacio.
Estos números cuánticos no pueden tomar cualquier valor. Están restringidos por reglas específicas. Por ejemplo, l puede tomar valores de 0 a n-1. ml puede tomar valores de -l a +l.
Implicaciones y Orbitales Atómicos
Las soluciones a la ecuación de Schrödinger predicen los orbitales atómicos. Estos orbitales son regiones del espacio. En estas regiones, existe una alta probabilidad de encontrar el electrón.
Los orbitales se clasifican según sus números cuánticos. Los orbitales s son esféricamente simétricos. Los orbitales p tienen forma de mancuerna. Los orbitales d y f tienen formas más complejas.
Sugerencias para la Enseñanza
Comience con una revisión de la física clásica. Contraste con la física cuántica. Explique las limitaciones del modelo de Bohr. Introduzca la idea de la dualidad onda-partícula.
Utilice analogías para explicar los números cuánticos. Por ejemplo, compare los niveles de energía con los escalones de una escalera. Visualice los orbitales utilizando software o modelos 3D.
Enfatice la importancia de la probabilidad. Explique que no podemos conocer la posición exacta del electrón. Solo podemos determinar la probabilidad de encontrarlo en una región del espacio.
Conceptos Erróneos Comunes
Los estudiantes a menudo confunden los orbitales con órbitas. Aclare que los orbitales son regiones de probabilidad. No son trayectorias definidas.
Otro error común es pensar que los electrones giran alrededor del núcleo. Explique que el modelo cuántico describe un comportamiento más complejo. Es diferente de la imagen clásica de electrones orbitando.
Algunos estudiantes creen que los orbitales están ocupados por múltiples electrones. Recuerde el principio de exclusión de Pauli. Este principio establece que cada orbital puede contener como máximo dos electrones. Estos electrones deben tener espines opuestos.
Haciendo el Concepto Atractivo
Utilice simulaciones interactivas para explorar los orbitales. Permita a los estudiantes modificar los números cuánticos. Observe cómo cambian las formas de los orbitales.
Organice debates sobre las implicaciones de la mecánica cuántica. Discuta sobre las tecnologías basadas en estos principios. Como los láseres y los semiconductores.
Proponga proyectos de investigación sobre aplicaciones de la espectroscopia atómica. Esta herramienta identifica elementos y compuestos. Analizando la luz que emiten o absorben.