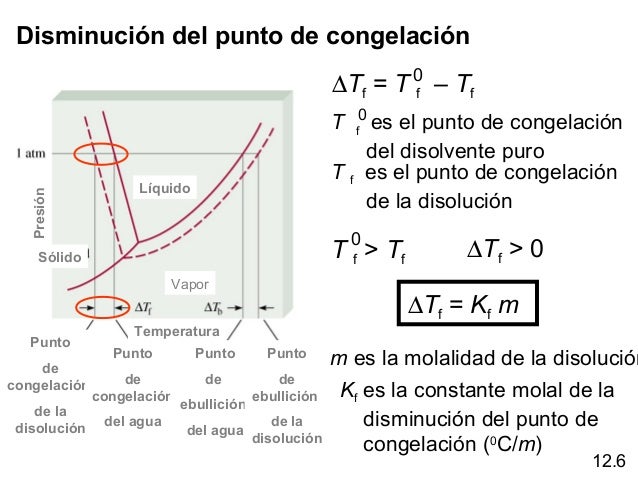
Disminución Del Punto De Congelación Definicion

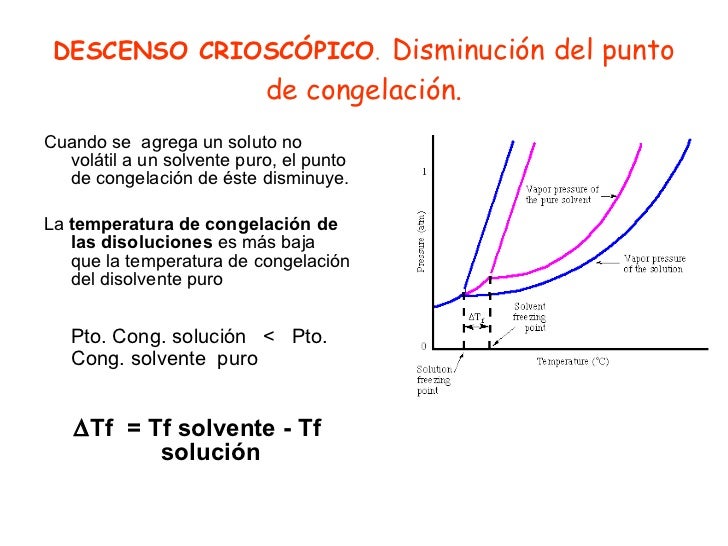
La disminución del punto de congelación es un fenómeno físico que se observa cuando se añade un soluto a un disolvente. El resultado es que la temperatura a la cual el disolvente se congela disminuye. Esto significa que la mezcla se congela a una temperatura más baja que el disolvente puro.
Definición Formal
La disminución del punto de congelación, también conocida como descenso crioscópico, es una propiedad coligativa. Las propiedades coligativas son aquellas que dependen únicamente de la cantidad de partículas de soluto presentes en una disolución. No dependen de la naturaleza química del soluto.
Formalmente, se define como la diferencia entre el punto de congelación del disolvente puro y el punto de congelación de la disolución.
Explicación Detallada
Para entender este fenómeno, imaginemos agua pura. A 0°C, las moléculas de agua tienen la energía cinética suficiente para formar enlaces entre sí y formar cristales de hielo. Este es el proceso de congelación.
Ahora, añadamos sal al agua. Las partículas de sal (iones de sodio y cloruro) se interponen entre las moléculas de agua. Esto dificulta que las moléculas de agua se unan y formen la estructura cristalina del hielo.
Por lo tanto, se necesita una temperatura más baja para que las moléculas de agua tengan suficiente energía cinética para superar la interferencia de las partículas de sal y congelarse. Es por eso que el punto de congelación disminuye.
Fórmula Matemática
La disminución del punto de congelación se puede calcular utilizando la siguiente fórmula:
ΔTf = Kf * m * i
Donde:
- ΔTf es la disminución del punto de congelación (en °C).
- Kf es la constante crioscópica del disolvente (en °C kg/mol). Esta constante es específica para cada disolvente. Por ejemplo, para el agua, Kf es 1.86 °C kg/mol.
- m es la molalidad de la disolución (en mol/kg). La molalidad se define como el número de moles de soluto por kilogramo de disolvente.
- i es el factor de Van't Hoff. Este factor representa el número de partículas en las que se disocia un soluto en disolución. Para solutos que no se disocian (como la glucosa), i = 1. Para solutos iónicos que se disocian (como la sal, NaCl), i es aproximadamente igual al número de iones producidos por unidad de fórmula (para NaCl, i ≈ 2).
Ejemplos
Ejemplo 1: Añadir sal a las carreteras en invierno. Al añadir sal a las carreteras, se disminuye el punto de congelación del agua. Esto ayuda a evitar que el agua se congele y forme hielo, lo que hace que las carreteras sean más seguras.
Ejemplo 2: Hacer helado casero. En muchas recetas de helado casero, se utiliza sal para enfriar la mezcla de helado. La sal disminuye el punto de congelación del agua, lo que permite alcanzar temperaturas más bajas y congelar el helado.
Ejemplo 3: Anticongelante en los coches. El anticongelante, que generalmente contiene etilenglicol, se añade al agua del radiador de un coche para disminuir su punto de congelación. Esto evita que el agua se congele en climas fríos y dañe el motor.
Aplicaciones Reales
La disminución del punto de congelación tiene muchas aplicaciones prácticas en diversos campos:
- Industria alimentaria: Conservación de alimentos, elaboración de helados.
- Industria química: Determinación de masas moleculares, estudio de disoluciones.
- Transporte: Deshielo de carreteras y pistas de aterrizaje.
- Medicina: Criopreservación de tejidos y órganos.
La comprensión de la disminución del punto de congelación es crucial en muchas disciplinas científicas y tecnológicas. Su estudio permite desarrollar soluciones innovadoras para diversos problemas, desde la seguridad vial hasta la conservación de alimentos y la medicina regenerativa.