Determinacion Del Punto Isoelectrico De Las Proteinas

Para determinar el punto isoeléctrico (pI) de una proteína, se requiere un enfoque sistemático. Este enfoque minimiza errores y maximiza la precisión.
Comprender el Problema
Primero, identifica la proteína específica. ¿Qué aminoácidos la componen? Investiga su estructura primaria y posibles modificaciones postraduccionales. Estas modificaciones pueden influir en su carga.
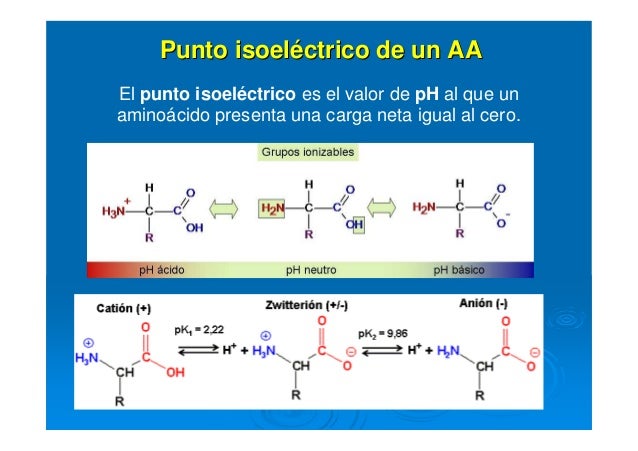
Segundo, define el pI. El pI es el pH al cual la proteína tiene carga neta cero. Comprende que la carga de una proteína depende del pH del entorno.
Recopilación de Información Relevante
Revisa la literatura científica existente. Busca información sobre el pI de la proteína específica o proteínas similares. Bases de datos como UniProt pueden ser útiles.
Consulta tablas de valores de pKa de los aminoácidos. Estos valores son esenciales para calcular la carga de la proteína a diferentes pHs. Recuerda que los grupos amino y carboxilo terminales también contribuyen a la carga.
Identifica cualquier residuo modificable. Considera fosforilaciones, glicosilaciones o acetilaciones. Estas modificaciones pueden alterar significativamente el pI.
Desarrollo de Posibles Soluciones
Enfoque Teórico: Cálculo Manual. Utiliza las ecuaciones de Henderson-Hasselbalch. Calcula la carga de cada aminoácido ionizable a diferentes pHs. Suma las cargas para obtener la carga neta de la proteína.
Busca dos valores de pH cercanos donde la carga neta cambie de positiva a negativa. Interpola entre estos valores para estimar el pI. Este método es preciso pero requiere tiempo.
Enfoque Teórico: Software de Simulación. Utiliza programas bioinformáticos. Estos programas predice el pI basándose en la secuencia de aminoácidos. Algunos programas consideran modificaciones postraduccionales.
Los programas como ExPASy's ProtParam tool son ejemplos de software disponibles. Asegúrate de ingresar la secuencia correcta. Verifica que los parámetros del programa sean apropiados.
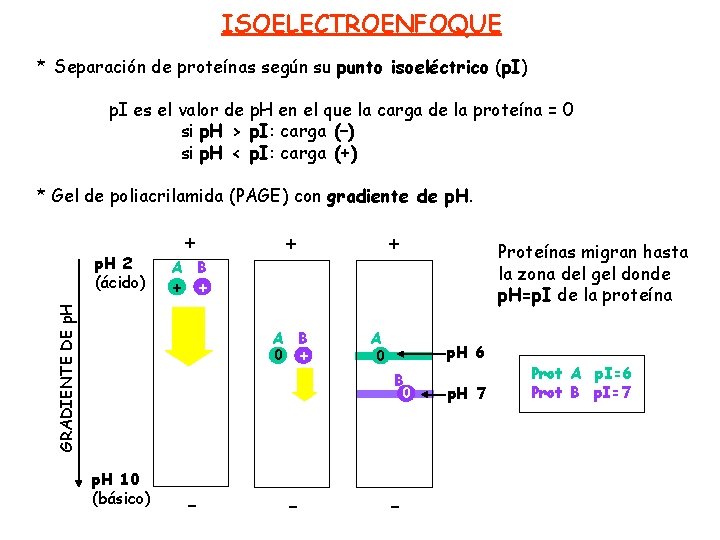
Enfoque Experimental: Enfoque Isoeléctrico (IEF). Realiza un IEF. Separa la proteína en un gradiente de pH. La proteína migrará hasta alcanzar su pI.
Utiliza geles de poliacrilamida con un gradiente de pH establecido. La proteína se concentrará en la banda correspondiente a su pI. Este método requiere equipo especializado.
Enfoque Experimental: Cromatografía de Intercambio Iónico. Utiliza cromatografía de intercambio iónico. Eluye la proteína utilizando un gradiente de pH. El pH al que la proteína se eluye corresponde a su pI.
Verificación de la Respuesta Final
Compara los resultados de los diferentes enfoques. ¿El pI calculado teóricamente coincide con el pI determinado experimentalmente? Discrepancias significativas sugieren errores.
Evalúa la validez de los datos experimentales. ¿El IEF produjo bandas nítidas y bien definidas? ¿El gradiente de pH en la cromatografía fue preciso? Problemas con el experimento pueden afectar la precisión.
Considera factores que puedan influir en el pI. La fuerza iónica de la solución puede afectar el pI. La temperatura también puede influir en la ionización de los grupos funcionales.
Si los resultados son inconsistentes, revisa cada paso. Verifica la secuencia de aminoácidos. Confirma los valores de pKa utilizados. Repite los experimentos si es necesario.
Finalmente, documenta todos los pasos y resultados. Describe los métodos utilizados. Explica cualquier discrepancia encontrada. Presenta una conclusión clara y concisa sobre el pI determinado.