Definicion De Reaccion De Sustitucion Simple
Vamos a definir una reacción de sustitución simple. Lo haremos paso a paso. Analizaremos cada componente.
Parte 1: ¿Qué es una reacción química?
Una reacción química es un proceso. Se transforman sustancias en otras. Los enlaces entre átomos se rompen y se forman.
Parte 2: Tipos de Reacciones Químicas
Existen muchos tipos de reacciones químicas. Incluyen la síntesis, descomposición, combustión. También están las reacciones de sustitución, entre otras.
Parte 3: Reacción de Sustitución
Una reacción de sustitución implica el reemplazo. Un átomo o grupo de átomos reemplaza a otro. Ocurre en un compuesto.
Parte 4: Reacción de Sustitución Simple (o Desplazamiento Simple)
La reacción de sustitución simple tiene una característica principal. Un elemento reemplaza a otro. Esto ocurre en un compuesto.
Parte 5: Componentes de una Reacción de Sustitución Simple
Identificamos dos componentes clave. Un elemento libre y un compuesto. El elemento libre es más reactivo.
Parte 6: Reactividad
La reactividad es crucial. Un elemento más reactivo desplaza a uno menos reactivo. Esto se basa en la serie de actividad.
Parte 7: Serie de Actividad
La serie de actividad es una lista. Organiza los metales según su reactividad. Un metal superior desplaza a uno inferior.
Parte 8: Ejemplo de Reacción de Sustitución Simple
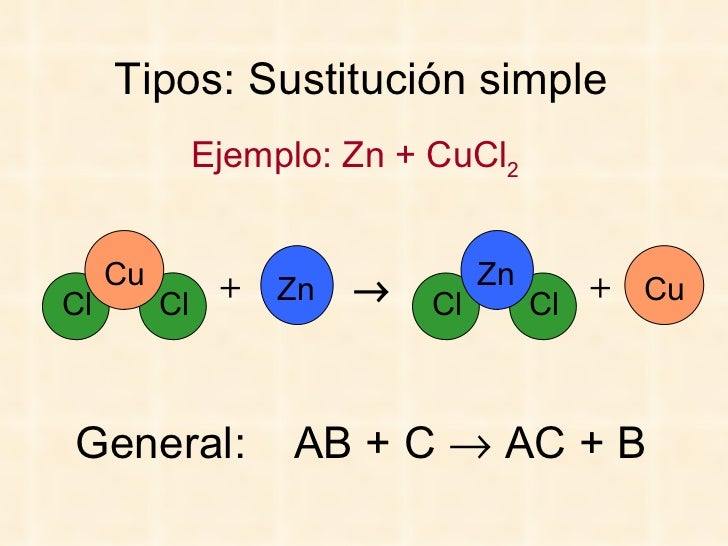
Consideremos el zinc (Zn) y el sulfato de cobre (CuSO4). El zinc es más reactivo que el cobre. El zinc desplaza al cobre del sulfato.
Parte 9: La Reacción
La reacción se escribe así: Zn + CuSO4 → ZnSO4 + Cu. El zinc ahora está en el sulfato de zinc. El cobre queda libre.
Parte 10: Observaciones
Podemos observar cambios en la reacción. El sulfato de cobre es azul. El sulfato de zinc es incoloro. El cobre metálico se deposita.
Parte 11: Otro Ejemplo
Consideremos el cloro (Cl2) y el bromuro de sodio (NaBr). El cloro es más reactivo que el bromo. El cloro desplaza al bromo.
Parte 12: La Reacción (Segundo Ejemplo)
La reacción se escribe así: Cl2 + 2NaBr → 2NaCl + Br2. El cloro forma cloruro de sodio. El bromo se libera.
Parte 13: No Todas las Reacciones Ocurren
Si el elemento libre es menos reactivo, no habrá reacción. Por ejemplo, el cobre no desplaza al zinc del sulfato de zinc.
Parte 14: Resumen de la Definición
Una reacción de sustitución simple es un tipo de reacción química. Un elemento reemplaza a otro. Ocurre en un compuesto, basado en la reactividad.
Parte 15: Definición Formal
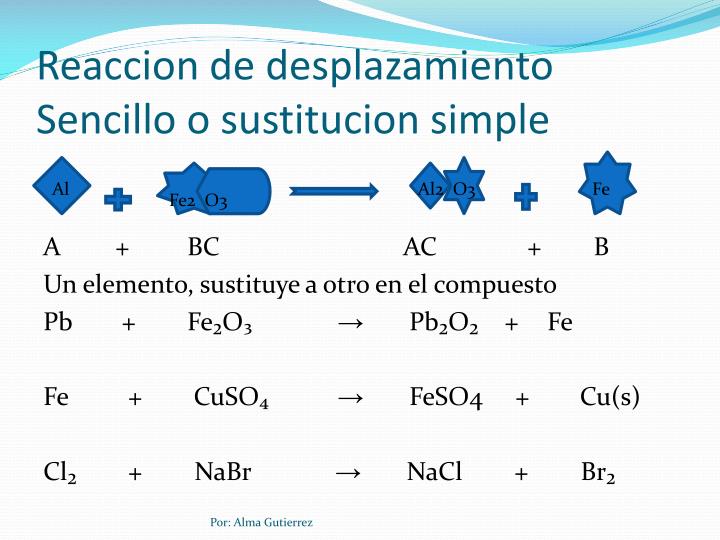
Una reacción de sustitución simple (también llamada reacción de desplazamiento simple) es una reacción química en la cual un elemento reemplaza a otro elemento dentro de un compuesto. Este proceso está impulsado por la diferencia en la reactividad de los elementos involucrados, donde un elemento más reactivo desplaza a un elemento menos reactivo. Se representa generalmente como: A + BC → AC + B, donde A es un elemento, BC es un compuesto, y B es el elemento desplazado.