Cual Es La Representacion De Lewis
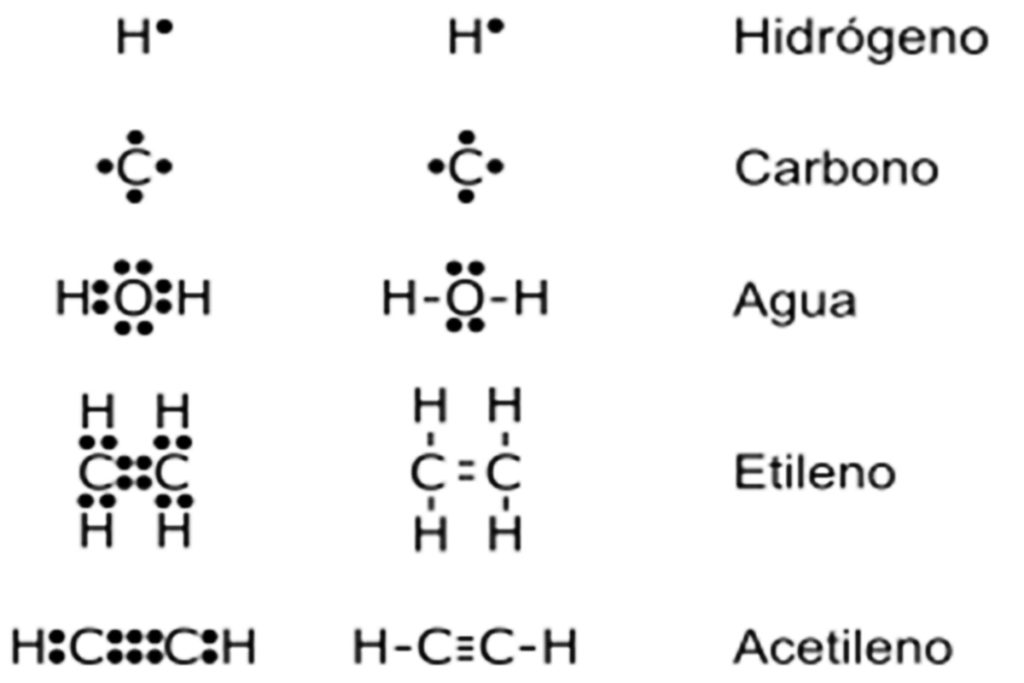
¡Hola a todos los aprendices visuales! Vamos a sumergirnos en el mundo de las representaciones de Lewis. Imaginen que cada átomo es una persona en una fiesta. Algunos quieren compartir sus dulces (electrones) para sentirse completos.
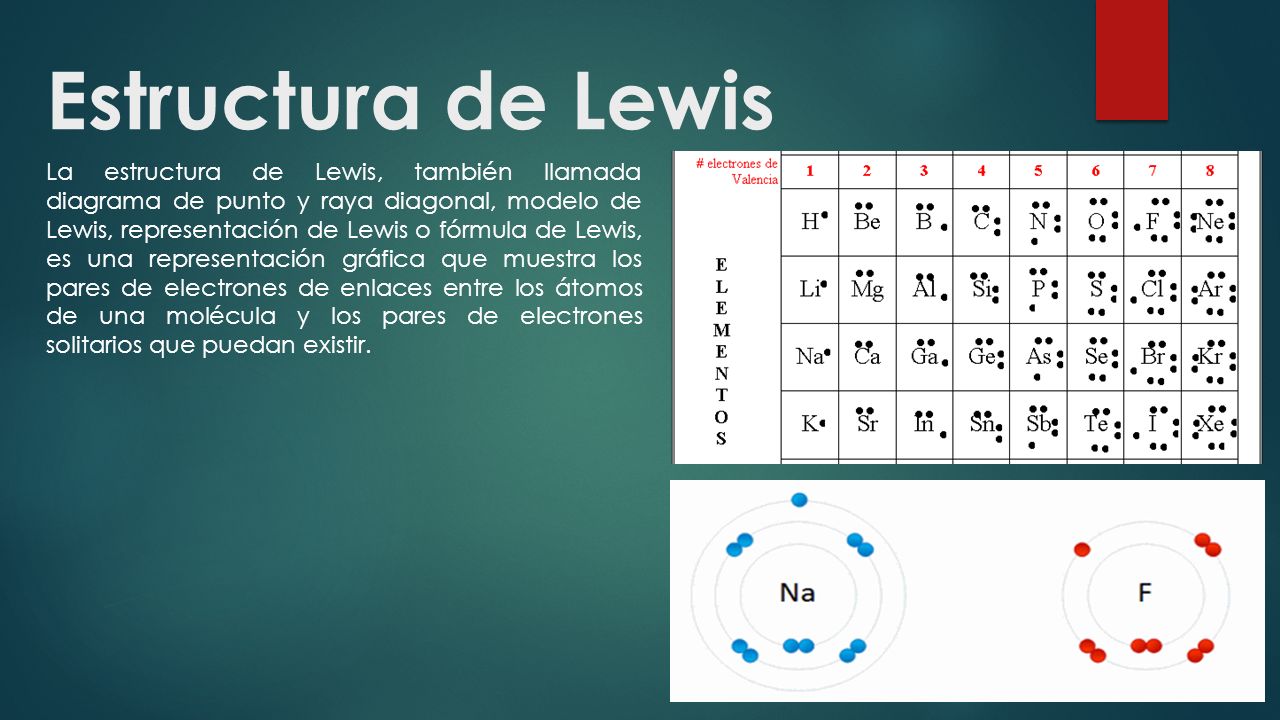
Las representaciones de Lewis son como diagramas que nos muestran cómo estas "personas" (átomos) comparten sus "dulces" (electrones) para formar enlaces. Es una forma visual de entender cómo se unen los átomos.
Entendiendo los Elementos Clave
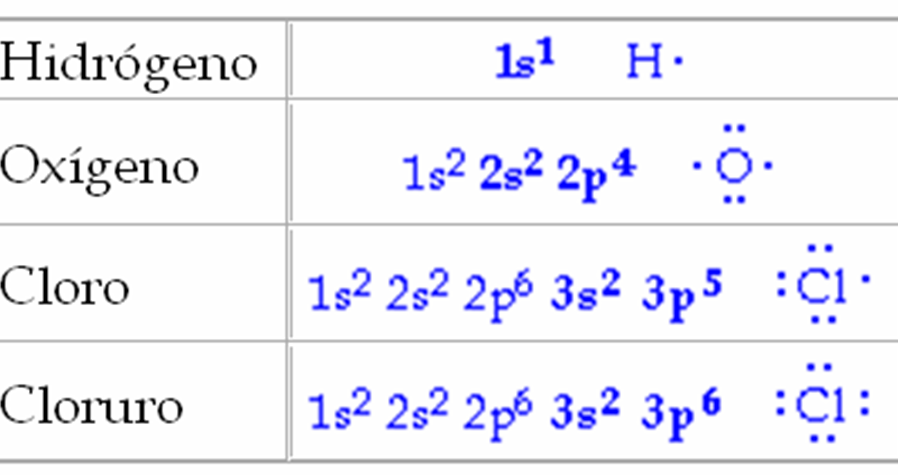
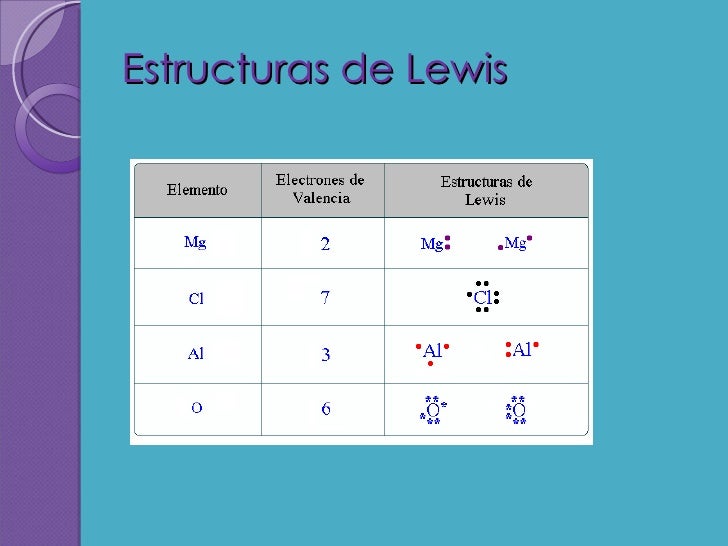
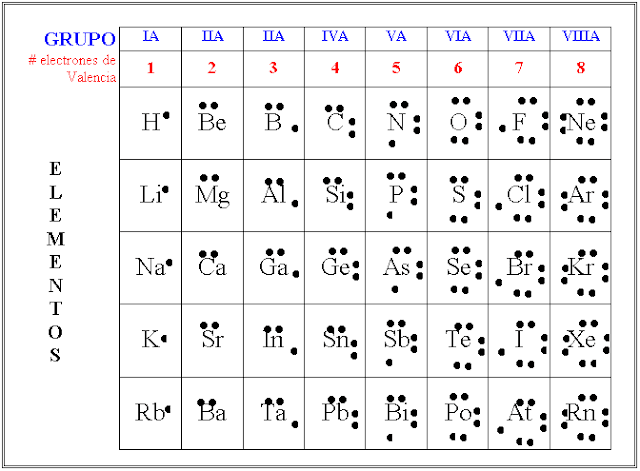
Primero, necesitamos entender a los jugadores principales. Estos son los elementos químicos. Cada elemento tiene una cierta cantidad de electrones de valencia. Estos son los electrones en la capa más externa del átomo, y son los que participan en los enlaces.
Piensa en los electrones de valencia como los dulces que cada persona trae a la fiesta. Algunos traen pocos, otros muchos. Por ejemplo, el oxígeno tiene 6 electrones de valencia. El sodio, por otro lado, tiene solo 1.
Para visualizarlo, imaginemos que dibujamos un punto alrededor del símbolo del elemento por cada electrón de valencia. Así, el oxígeno tendría seis puntos alrededor de la "O", y el sodio tendría solo uno alrededor de la "Na".
La Regla del Octeto
La mayoría de los átomos "quieren" tener 8 electrones de valencia en su capa más externa. Esta es la famosa regla del octeto. Es como si cada persona quisiera tener 8 dulces en su plato para estar feliz.
Hay excepciones, por supuesto. El hidrógeno solo necesita 2 electrones. Es como si una persona se conformara con tener solo dos dulces en su plato. Piensa en ello como una regla general, no una ley inquebrantable.
Creando Enlaces
Ahora, veamos cómo se forman los enlaces. Los átomos comparten electrones para completar sus octetos. Hay dos tipos principales de enlaces: enlaces iónicos y enlaces covalentes.
Un enlace iónico es como si una persona le diera todos sus dulces a otra. Esto sucede cuando hay una gran diferencia en la electronegatividad entre los átomos. Por ejemplo, el sodio (Na) le da su electrón al cloro (Cl) para formar cloruro de sodio (sal de mesa).
Un enlace covalente es como si dos personas compartieran sus dulces. Esto sucede cuando los átomos tienen electronegatividades similares. Por ejemplo, dos átomos de oxígeno comparten electrones para formar una molécula de oxígeno (O2).
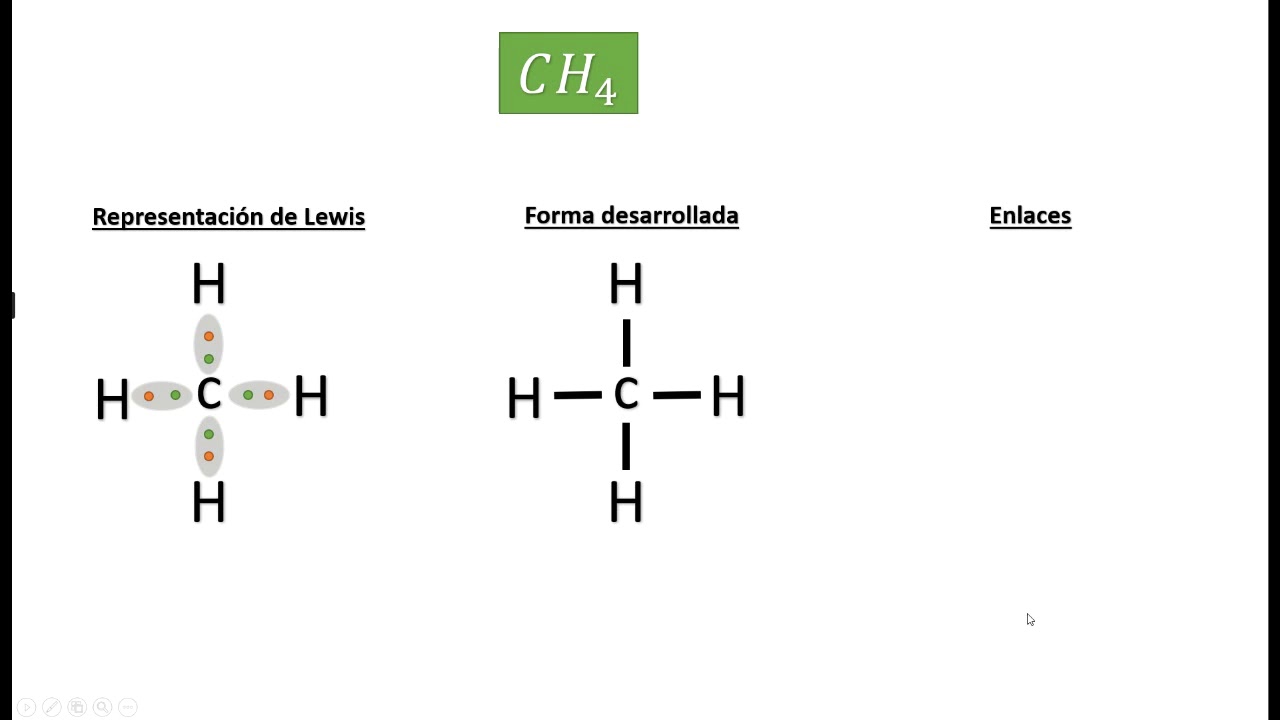
Dibujando las Representaciones de Lewis
Para dibujar una representación de Lewis, sigue estos pasos:
- Cuenta el número total de electrones de valencia en la molécula.
- Dibuja los símbolos de los átomos, conectándolos con líneas (cada línea representa un par de electrones compartidos).
- Coloca los electrones restantes como pares solitarios alrededor de los átomos para completar los octetos (o dueto para el hidrógeno).
Por ejemplo, para dibujar la representación de Lewis del agua (H2O), tenemos 2 átomos de hidrógeno (cada uno con 1 electrón) y 1 átomo de oxígeno (con 6 electrones). Esto da un total de 8 electrones.
El oxígeno se coloca en el centro, con dos átomos de hidrógeno unidos a él. Cada enlace H-O representa 2 electrones. Los 4 electrones restantes se colocan como dos pares solitarios alrededor del oxígeno.
Ejemplos Adicionales
Dióxido de carbono (CO2): El carbono tiene 4 electrones de valencia y cada oxígeno tiene 6. Total: 4 + (2 x 6) = 16 electrones. El carbono se une a cada oxígeno con un enlace doble. Esto satisface el octeto para cada átomo.
Amoníaco (NH3): El nitrógeno tiene 5 electrones de valencia y cada hidrógeno tiene 1. Total: 5 + (3 x 1) = 8 electrones. El nitrógeno se une a cada hidrógeno con un enlace simple, dejando un par solitario en el nitrógeno.
Las representaciones de Lewis son herramientas muy útiles para predecir la estructura y las propiedades de las moléculas. Practica dibujando representaciones de Lewis para diferentes moléculas y te convertirás en un experto en visualizar el mundo molecular.