Configuración Electrónica De Los Elementos Químicos
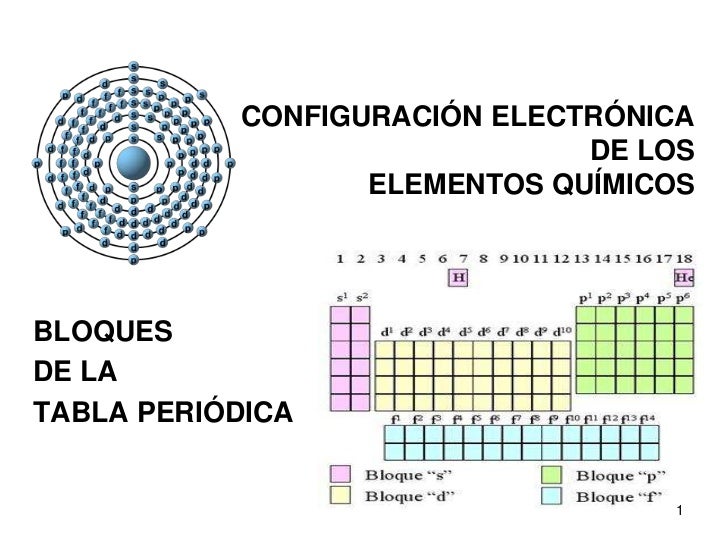
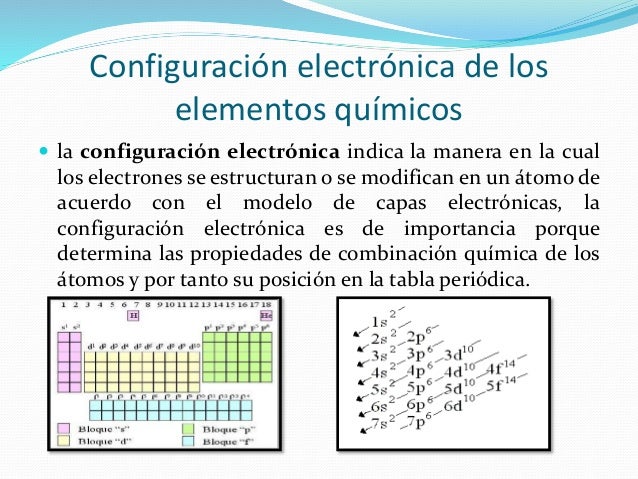
La configuración electrónica de un elemento químico describe cómo se distribuyen los electrones en los diferentes niveles y subniveles de energía alrededor del núcleo del átomo. En pocas palabras, es un "mapa" de dónde se encuentran los electrones.
Para entenderla, debemos recordar algunos conceptos clave:
- Niveles de energía: Son como "pisos" alrededor del núcleo. Se numeran del 1 en adelante (n=1, n=2, n=3, etc.). Cuanto mayor es el número, más lejos del núcleo y mayor la energía.
- Subniveles de energía: Cada nivel de energía se divide en subniveles, designados por las letras s, p, d, y f.
- Orbitales: Cada subnivel contiene uno o más orbitales, que son regiones del espacio donde es probable encontrar un electrón.
Cada orbital puede contener un máximo de dos electrones (Principio de Exclusión de Pauli). Los subniveles pueden contener el siguiente número máximo de electrones:
- s: 2 electrones
- p: 6 electrones
- d: 10 electrones
- f: 14 electrones
La configuración electrónica se escribe indicando primero el nivel de energía (el número), luego el subnivel (la letra) y finalmente el número de electrones en ese subnivel como un superíndice.
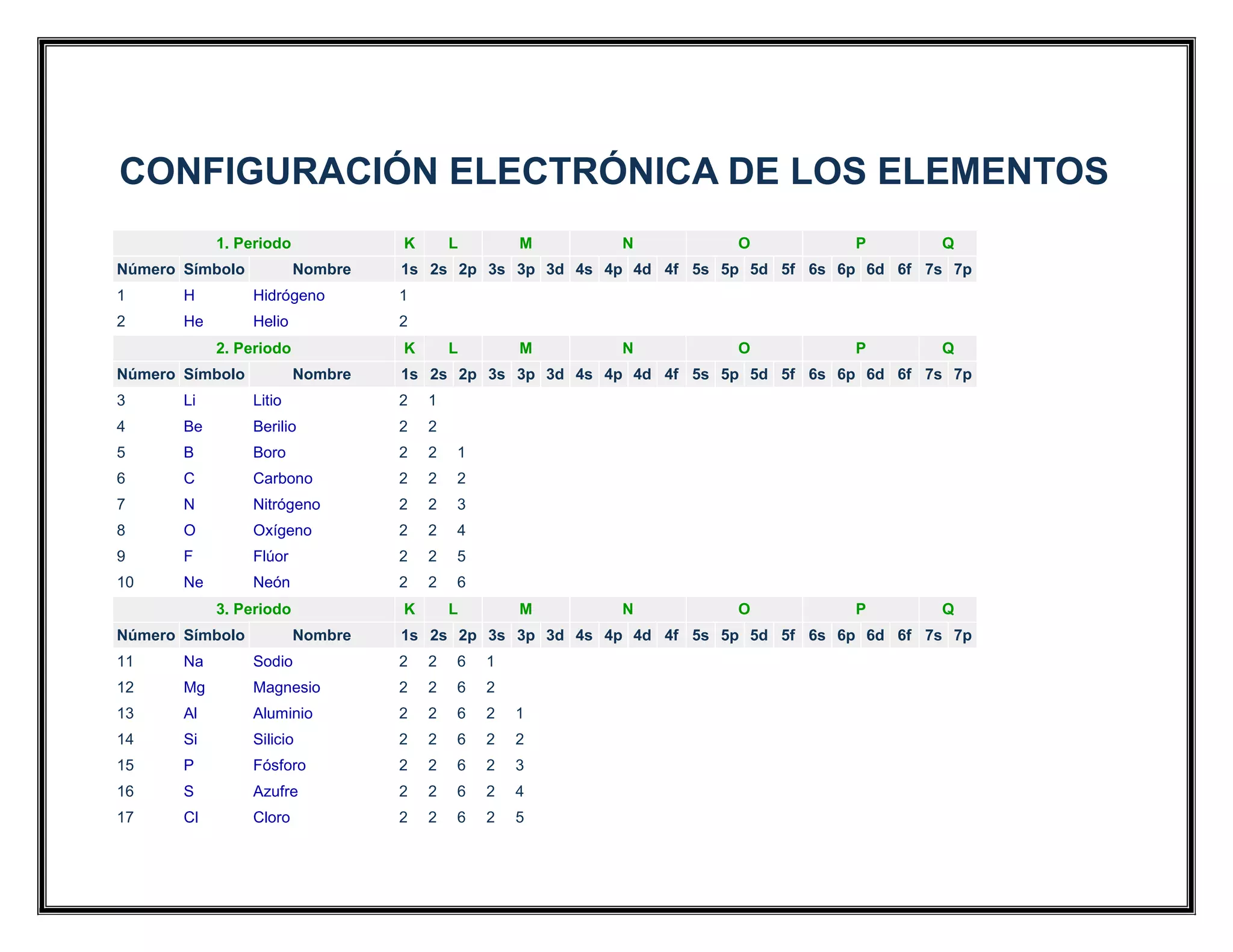
Ejemplo: El hidrógeno (H) tiene un solo electrón. Su configuración electrónica es 1s1. Esto significa que tiene 1 electrón en el subnivel "s" del nivel de energía 1.
Otro ejemplo: El helio (He) tiene dos electrones. Su configuración electrónica es 1s2. El subnivel "s" del nivel 1 está ahora completo.
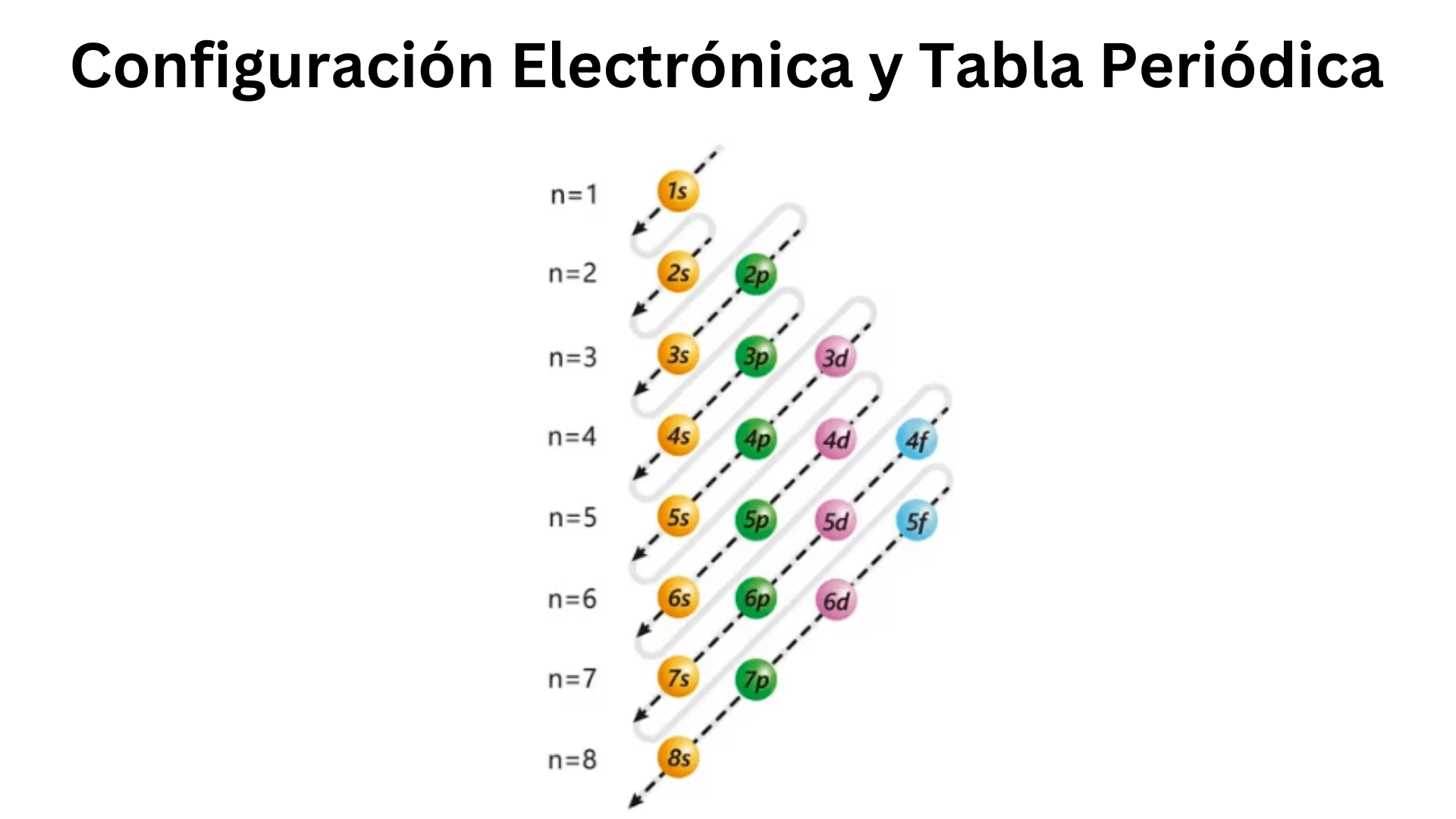
Para elementos más complejos, seguimos un orden de llenado de los subniveles de energía, conocido como la regla de las diagonales o diagrama de Moeller. Este diagrama nos indica el orden en el que se van llenando los orbitales: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, etc.
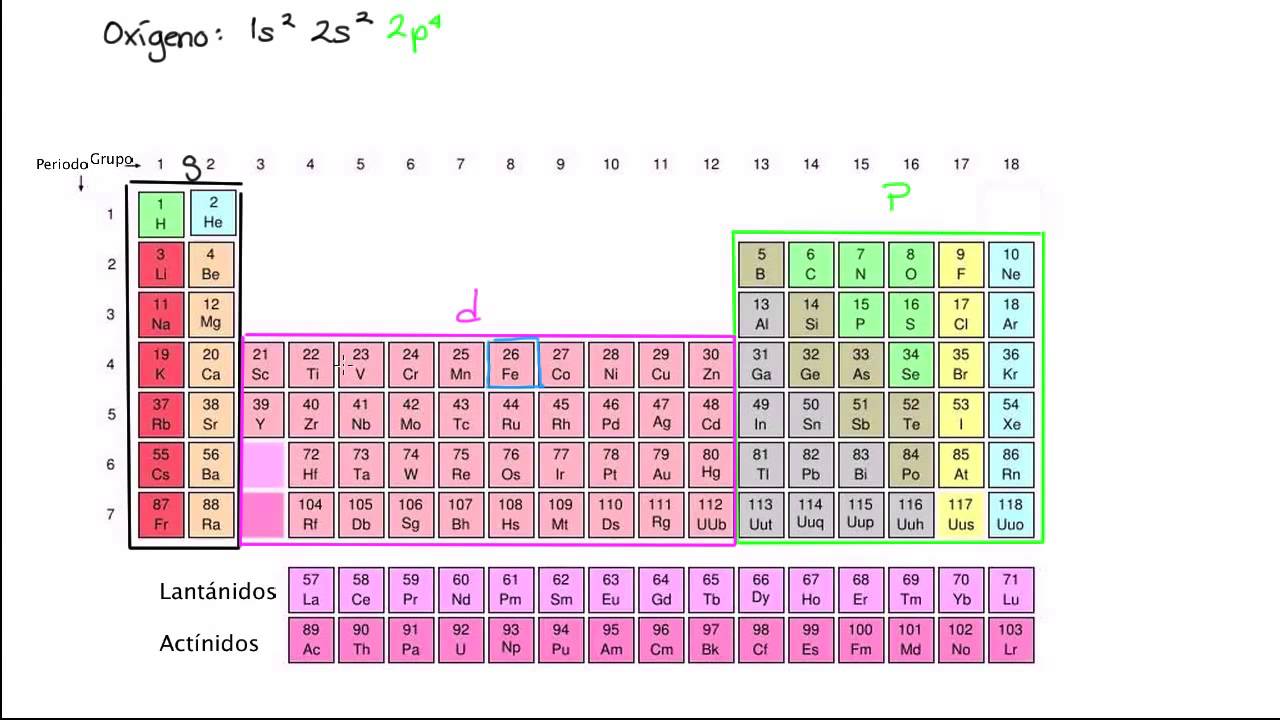
Ejemplo: El oxígeno (O) tiene 8 electrones. Siguiendo la regla de las diagonales, su configuración electrónica es 1s2 2s2 2p4. Esto significa: 2 electrones en 1s, 2 electrones en 2s, y 4 electrones en 2p.
La configuración electrónica es crucial porque determina las propiedades químicas de un elemento y cómo interactúa con otros elementos para formar compuestos.