Conceptos Basicos Para Entender Las Leyes De Los Gases
Las leyes de los gases describen el comportamiento de los gases ideales en relación con la presión, el volumen, la temperatura y la cantidad de sustancia (generalmente medida en moles). En esencia, explican cómo estas propiedades se relacionan entre sí.
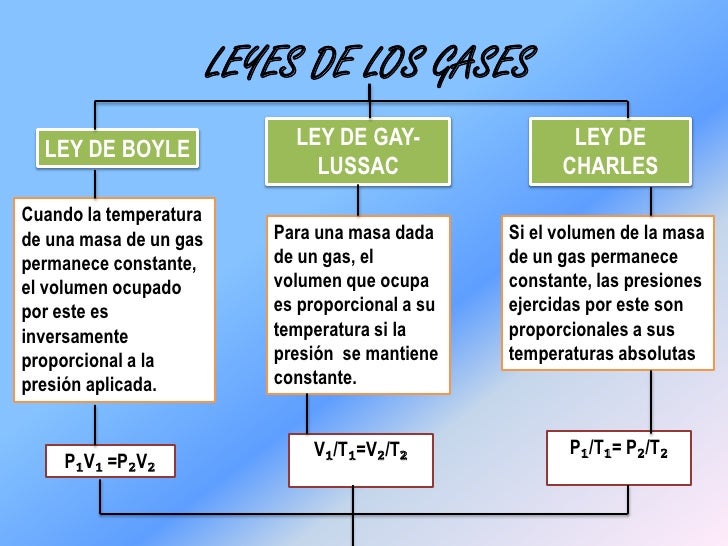
Ley de Boyle: Esta ley establece que, a temperatura constante, la presión de un gas es inversamente proporcional a su volumen. En otras palabras, si aumentas la presión sobre un gas, su volumen disminuirá proporcionalmente. Matemáticamente, se expresa como: P₁V₁ = P₂V₂. Por ejemplo, si tienes un gas en un recipiente de 1 litro a 2 atmósferas de presión y reduces el volumen a 0.5 litros, la presión aumentará a 4 atmósferas.
Ley de Charles: Esta ley indica que, a presión constante, el volumen de un gas es directamente proporcional a su temperatura absoluta (medida en Kelvin). Si calientas un gas, su volumen aumentará. La fórmula es: V₁/T₁ = V₂/T₂. Por ejemplo, si tienes un globo a 27°C (300 K) y lo calientas a 57°C (330 K), el volumen del globo aumentará en un factor de 330/300 = 1.1.
Ley de Gay-Lussac: Esta ley establece que, a volumen constante, la presión de un gas es directamente proporcional a su temperatura absoluta. Si aumentas la temperatura de un gas en un recipiente cerrado, la presión aumentará. La fórmula es: P₁/T₁ = P₂/T₂. Imaginen un aerosol. Si lo expones al calor, la temperatura aumentará y con ella la presión interna, pudiendo llegar a explotar si sobrepasa el límite del envase.
Ley de Avogadro: Esta ley afirma que, a temperatura y presión constantes, el volumen de un gas es directamente proporcional a la cantidad de sustancia (número de moles). Más moles de gas significan mayor volumen. Esto se expresa como: V₁/n₁ = V₂/n₂. Si inflas un globo, añades más moles de aire y el volumen aumenta.
Estas leyes se combinan en la Ley de los Gases Ideales: PV = nRT, donde R es la constante universal de los gases. Es fundamental entenderlas para predecir el comportamiento de los gases en diversas aplicaciones.
Aplicaciones prácticas: Las leyes de los gases son cruciales para el diseño de motores de combustión interna (donde la expansión de gases calientes genera trabajo) y en la meteorología (para predecir el comportamiento de las masas de aire).




