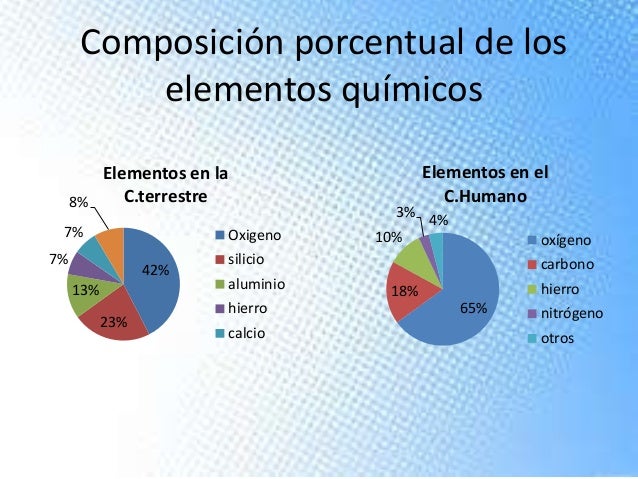
Composicion Porcentual De Los Compuestos Quimicos

Calcular la composición porcentual de un compuesto químico es determinar el porcentaje en masa de cada elemento que lo conforma. Es una herramienta fundamental en química para identificar compuestos y verificar su pureza.
Paso 1: Escribe la Fórmula Química
Primero, necesitas la fórmula química del compuesto. Esta fórmula te dice qué elementos están presentes y cuántos átomos de cada elemento hay en una molécula. Por ejemplo, la fórmula del agua es H2O, lo que indica que hay dos átomos de hidrógeno (H) y un átomo de oxígeno (O).
Consideremos el ejemplo del cloruro de sodio (NaCl), la sal de mesa común. Su fórmula es sencilla: NaCl. Esta fórmula indica que hay un átomo de sodio (Na) y un átomo de cloro (Cl).
Paso 2: Encuentra las Masas Atómicas
Necesitarás una tabla periódica para encontrar las masas atómicas de cada elemento en el compuesto. La masa atómica es el peso de un átomo de ese elemento, expresado en unidades de masa atómica (uma). Usualmente, se encuentra debajo del símbolo del elemento en la tabla periódica.
Busca las masas atómicas de los elementos presentes en el compuesto. En nuestro ejemplo del NaCl, busca la masa atómica del sodio (Na) y del cloro (Cl) en la tabla periódica.
Para el sodio (Na), la masa atómica es aproximadamente 22.99 uma. Para el cloro (Cl), la masa atómica es aproximadamente 35.45 uma.
Paso 3: Calcula la Masa Molar del Compuesto
La masa molar es la masa de un mol de un compuesto. Para calcularla, suma las masas atómicas de todos los átomos en la fórmula química. Multiplica la masa atómica de cada elemento por el número de átomos de ese elemento en la fórmula.
En el caso del NaCl, la masa molar se calcula de la siguiente manera:
- Masa atómica del Na: 22.99 uma
- Masa atómica del Cl: 35.45 uma
Masa molar del NaCl = 22.99 + 35.45 = 58.44 g/mol (gramos por mol).
Paso 4: Calcula el Porcentaje de Cada Elemento
Para calcular el porcentaje de cada elemento, divide la masa total de cada elemento en el compuesto por la masa molar total del compuesto, y luego multiplica por 100%.
La fórmula es: Porcentaje del elemento = (Masa total del elemento / Masa molar del compuesto) x 100%
Calculando para el NaCl:
- Porcentaje de Na = (22.99 / 58.44) x 100% = 39.34%
- Porcentaje de Cl = (35.45 / 58.44) x 100% = 60.66%
Ejemplo Adicional: Agua (H2O)
Repitamos los pasos para el agua (H2O).
- Paso 1: Fórmula química: H2O
- Paso 2: Masas atómicas: H (1.01 uma), O (16.00 uma)
Paso 3: Masa molar del H2O = (2 x 1.01) + 16.00 = 18.02 g/mol
Paso 4: Composición porcentual:
- Porcentaje de H = (2.02 / 18.02) x 100% = 11.21%
- Porcentaje de O = (16.00 / 18.02) x 100% = 88.79%
En resumen, la composición porcentual nos da una valiosa información sobre la cantidad relativa de cada elemento en un compuesto, lo que facilita su identificación y análisis.