Como Saber Si Es Polar O No Polar

Entender la polaridad de una molécula es fundamental en química. Es clave para comprender las propiedades físicas y químicas de las sustancias. Aquí te presentamos una guía para saber si una molécula es polar o no polar, enfocada en cómo puedes explicarlo a tus estudiantes de manera efectiva.
Conceptos Clave: Electronegatividad y Momentos Dipolares
Comienza por revisar la electronegatividad. La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí en un enlace químico. Utiliza la escala de Pauling para ilustrar las diferencias entre los elementos. Por ejemplo, el oxígeno es mucho más electronegativo que el hidrógeno.
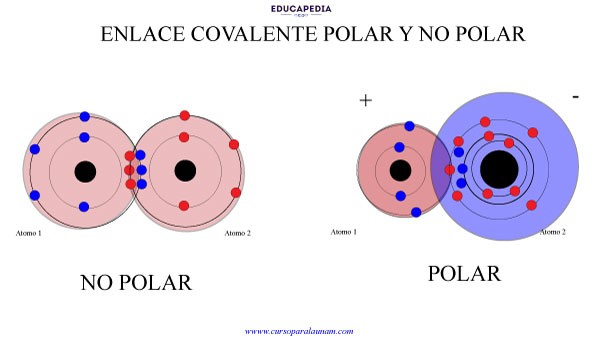
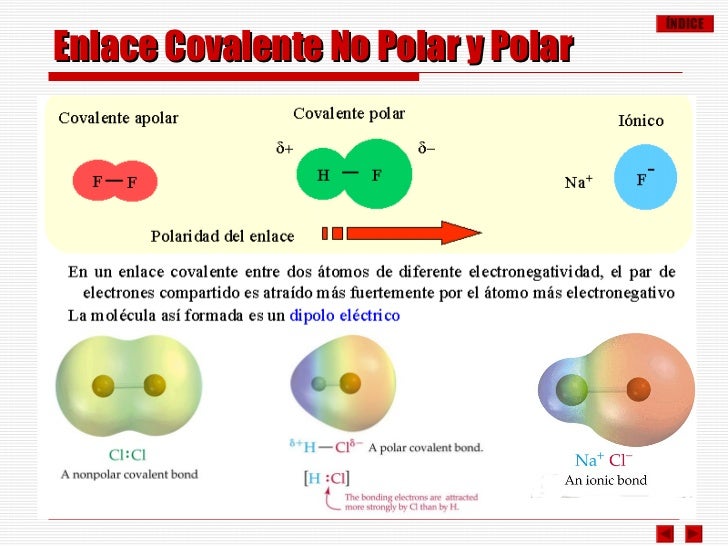
Explica que un enlace es polar si existe una diferencia significativa de electronegatividad entre los átomos enlazados. Esta diferencia crea un momento dipolar, representado por una flecha que apunta hacia el átomo más electronegativo. Si la diferencia de electronegatividad es muy pequeña, el enlace se considera no polar.
Es importante que los estudiantes comprendan la relación entre la diferencia de electronegatividad y el tipo de enlace. Un enlace con una gran diferencia será un enlace iónico. Una diferencia menor resultará en un enlace covalente polar. Una diferencia casi nula resulta en un enlace covalente no polar.
Geometría Molecular: La Clave para la Polaridad Molecular
La polaridad de los enlaces no es suficiente para determinar la polaridad de la molécula completa. La geometría molecular juega un papel crucial. Moléculas con enlaces polares pueden ser no polares si la geometría hace que los momentos dipolares se cancelen.
Considera el dióxido de carbono (CO2). Cada enlace C=O es polar. Sin embargo, la molécula es lineal, por lo que los momentos dipolares se anulan mutuamente. Por lo tanto, el CO2 es una molécula no polar.
En contraste, el agua (H2O) también tiene enlaces O-H polares. Pero, su forma es angular. Esto impide que los momentos dipolares se cancelen, resultando en una molécula polar.
Cómo Explicar en Clase: Consejos para Educadores
Utiliza modelos moleculares para ayudar a los estudiantes a visualizar la geometría. Esto hace que el concepto de cancelación de momentos dipolares sea más tangible. Hay kits de construcción molecular disponibles, o incluso pueden usar plastilina.
Emplea analogías. Por ejemplo, compara los momentos dipolares con "tirones de cuerda" en direcciones opuestas. Si los tirones son iguales y opuestos, la cuerda no se mueve (molécula no polar). Si un lado tira con más fuerza, la cuerda se mueve (molécula polar).
Resuelve ejemplos paso a paso. Comienza con moléculas sencillas como HCl, luego pasa a moléculas más complejas como amoníaco (NH3) y tetracloruro de carbono (CCl4). Involucra a los estudiantes preguntándoles sobre la electronegatividad y la geometría.
Errores Comunes y Cómo Evitarlos
Un error común es asumir que todos los enlaces polares automáticamente hacen que la molécula sea polar. Insiste en la importancia de la geometría molecular. Recuérdales que la simetría puede cancelar los momentos dipolares.
Otro error es confundir la electronegatividad con la carga formal. Explica claramente que la electronegatividad es una propiedad relativa, mientras que la carga formal es una carga hipotética basada en el número de electrones de valencia.
Muchos estudiantes tienen dificultades para visualizar la geometría molecular en tres dimensiones. Anima a usar software de visualización molecular en 3D. Estos programas pueden ayudarles a comprender la forma y la orientación de las moléculas.
Haciendo el Concepto Atractivo
Organiza debates. Pregunta a los estudiantes qué moléculas esperan que sean polares o no polares y por qué. Esto fomenta el pensamiento crítico y la discusión en grupo.
Realiza experimentos sencillos. Por ejemplo, puedes mostrar cómo un chorro de agua se desvía al acercarle una varilla cargada estáticamente. El agua es polar, mientras que otros líquidos no polares no se desvían.
Conecta la polaridad con aplicaciones del mundo real. Explica cómo la polaridad del agua afecta su capacidad para disolver diferentes sustancias. Menciona cómo los detergentes funcionan gracias a sus partes polares y no polares.
Al emplear estas estrategias, puedes ayudar a tus estudiantes a comprender la polaridad molecular de manera más clara y atractiva. Les proporcionas una base sólida para comprender conceptos más avanzados en química.