Como Calcular La Concentracion De Iones Hidrogeno

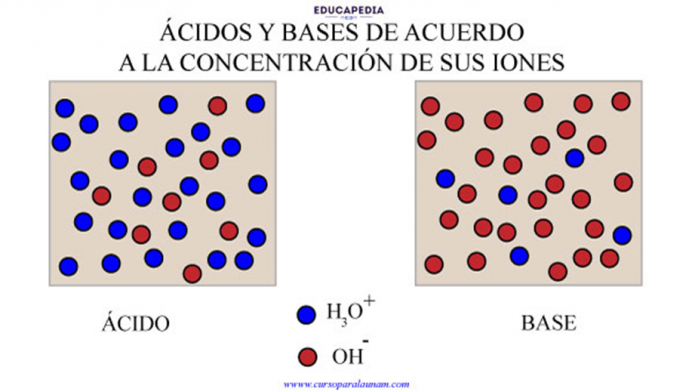
Calcular la concentración de iones hidrógeno (H+) es fundamental en química y biología, ya que determina la acidez o basicidad de una solución. Esta concentración, expresada generalmente en moles por litro (mol/L o M), influye en una amplia gama de procesos, desde reacciones químicas hasta la función enzimática en los seres vivos. Entender cómo calcularla es crucial para controlar y predecir el comportamiento de sistemas acuosos.
Cálculo Directo: Disociación de Ácidos Fuertes
Para ácidos fuertes, como el ácido clorhídrico (HCl), la disociación en agua es completa. Esto significa que cada molécula de ácido produce un ión H+. Por lo tanto, la concentración de H+ es igual a la concentración del ácido.
- Paso 1: Identifica la concentración del ácido fuerte. Por ejemplo, si tienes una solución de HCl 0.1 M.
- Paso 2: Asume que la concentración de H+ es igual a la concentración del ácido. En este caso, [H+] = 0.1 M.
Ejemplo: Si tienes una solución 0.05 M de ácido nítrico (HNO3), entonces [H+] = 0.05 M.
Cálculo Indirecto: Uso del pH
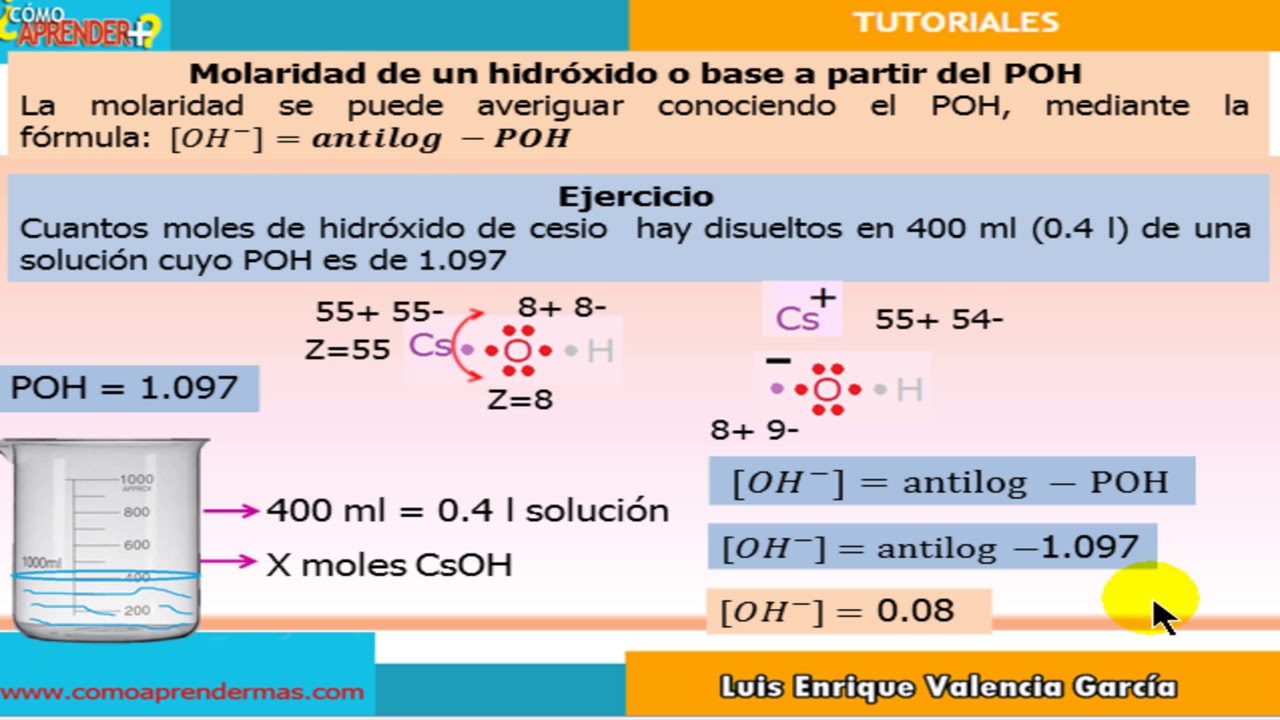
En muchos casos, la concentración de H+ no se conoce directamente, pero se proporciona el pH de la solución. El pH está relacionado con la concentración de H+ mediante la siguiente fórmula: pH = -log10[H+]. Para encontrar [H+] a partir del pH, necesitamos tomar el antilogaritmo (10 a la potencia negativa del pH):
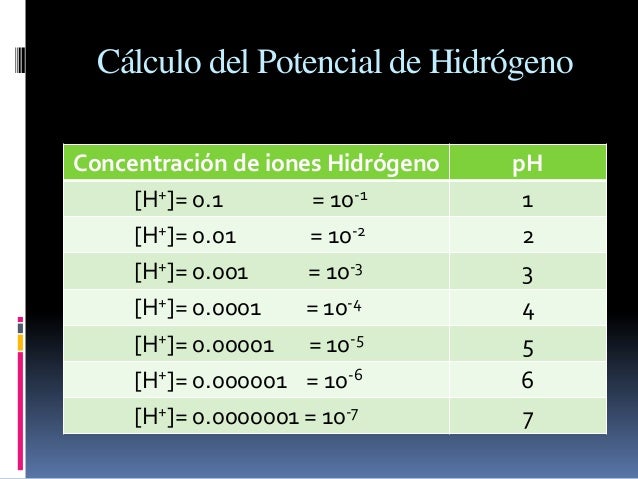
- Paso 1: Conoce el valor del pH. Por ejemplo, supongamos que el pH de una solución es 3.
- Paso 2: Aplica la fórmula: [H+] = 10-pH.
- Paso 3: Sustituye el valor del pH: [H+] = 10-3 M.
- Paso 4: Calcula el resultado: [H+] = 0.001 M.
Ejemplo: Si el pH de una muestra de agua es 7, entonces [H+] = 10-7 M, que es 0.0000001 M.
Consideraciones para Ácidos Débiles
El cálculo para ácidos débiles es más complejo ya que solo se disocian parcialmente. Requiere conocer la constante de acidez (Ka) y resolver una ecuación de equilibrio, lo cual está fuera del alcance de esta guía rápida. Sin embargo, recuerda que la concentración de H+ será siempre menor que la concentración inicial del ácido débil.