Como Calcular El Ph De Una Solucion
El pH es una medida de la acidez o la basicidad de una solución acuosa. Se expresa en una escala de 0 a 14. Un pH de 7 se considera neutro. Valores por debajo de 7 indican acidez, mientras que valores por encima de 7 indican basicidad (o alcalinidad).
Calcular el pH es fundamental en química, biología y otras ciencias. Entender cómo hacerlo nos permite predecir el comportamiento de soluciones y reacciones químicas.
Comprendiendo el Concepto de pH
El pH está directamente relacionado con la concentración de iones de hidrógeno (H+) en una solución. Matemáticamente, el pH se define como el logaritmo negativo en base 10 de la concentración de iones hidrógeno:
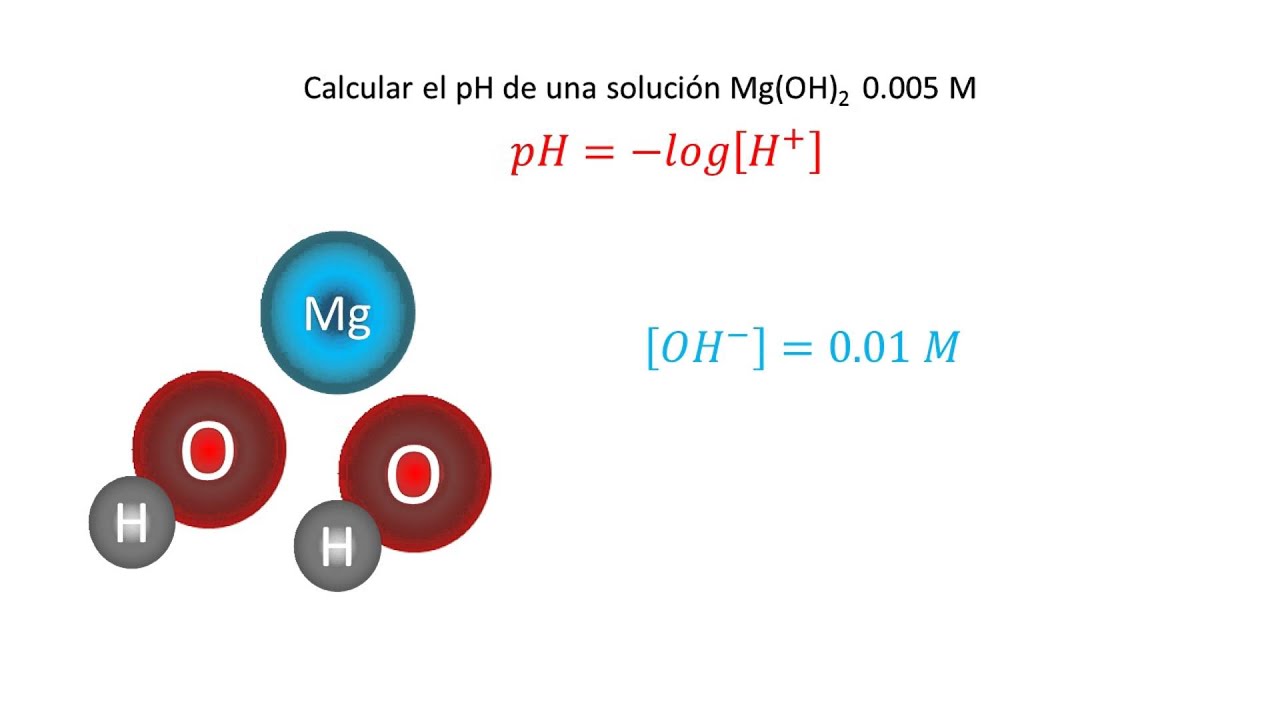
pH = -log10[H+]
Donde [H+] representa la concentración molar de iones hidrógeno. Recuerda que la concentración molar se expresa en moles por litro (mol/L).
Calculando el pH: Paso a Paso
Para calcular el pH, sigue estos pasos:
- Identifica la concentración de iones hidrógeno [H+]. Este valor debe ser proporcionado en el problema o puedes deducirlo si conoces la concentración de un ácido fuerte.
- Aplica la fórmula. Usa la fórmula pH = -log10[H+] para calcular el pH.
- Usa una calculadora. La mayoría de las calculadoras científicas tienen una función de logaritmo (log).
Ejemplo 1: Ácido Fuerte
Supongamos que tienes una solución de ácido clorhídrico (HCl) con una concentración de 0.01 M. El HCl es un ácido fuerte, lo que significa que se disocia completamente en agua para formar iones H+ y Cl-. Por lo tanto, [H+] = 0.01 M.
Aplicando la fórmula: pH = -log10(0.01) = 2. El pH de esta solución es 2, lo que indica que es una solución ácida.
Ejemplo 2: Concentración Expresada en Notación Científica
Si la concentración de iones hidrógeno es 1 x 10-5 M, entonces: pH = -log10(1 x 10-5) = 5. Esta solución también es ácida.
El pOH y su Relación con el pH
El pOH es una medida de la concentración de iones hidróxido (OH-) en una solución. Se define como: pOH = -log10[OH-].
El pH y el pOH están relacionados por la siguiente ecuación:
pH + pOH = 14
Esta ecuación es válida a 25°C. Si conoces el pOH, puedes calcular el pH restando el pOH de 14.
Ejemplo: Calculando el pH a partir del pOH
Si una solución tiene un pOH de 4, entonces: pH = 14 - 4 = 10. Esta solución es básica.
Ácidos y Bases Débiles
Los ácidos y bases débiles no se disocian completamente en agua. Para calcular el pH de una solución de un ácido o base débil, necesitas conocer la constante de disociación ácida (Ka) o la constante de disociación básica (Kb), respectivamente. El cálculo es más complejo e involucra el uso de una tabla ICE (Inicial, Cambio, Equilibrio) para determinar la concentración de H+ o OH- en el equilibrio.
Los cálculos para ácidos y bases débiles están fuera del alcance de esta explicación básica, pero es importante saber que requieren un enfoque diferente que los ácidos y bases fuertes.
Aplicaciones Prácticas
El cálculo del pH tiene muchas aplicaciones prácticas. Por ejemplo, en la agricultura, el pH del suelo es crucial para el crecimiento de las plantas. En la industria alimentaria, el pH afecta la conservación de los alimentos y el sabor. En la medicina, el pH de la sangre es un indicador importante de la salud. La industria cosmética también lo usa para formular productos compatibles con la piel.




