Cloruro De Sodio Propiedades Físicas Y Químicas
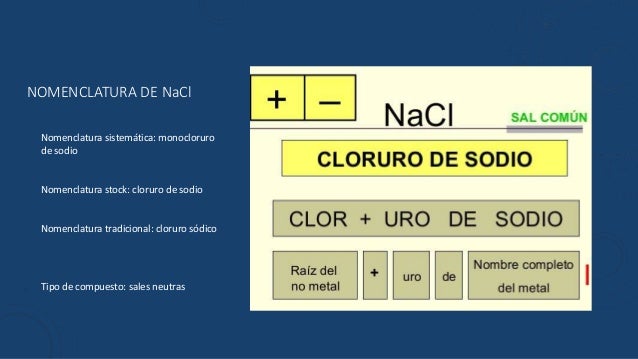
El cloruro de sodio, más conocido como sal común o sal de mesa, es un compuesto químico esencial para la vida y con una amplia variedad de aplicaciones industriales y culinarias. Su fórmula química es NaCl, lo que indica que está formado por un átomo de sodio (Na) y un átomo de cloro (Cl).
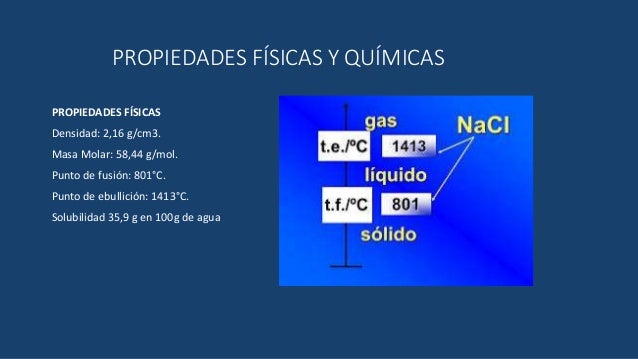
Propiedades Físicas del Cloruro de Sodio
Las propiedades físicas describen las características de una sustancia que se pueden observar o medir sin cambiar su composición química. Son propiedades inherentes al compuesto y ayudan a identificarlo y comprender su comportamiento.
Estado Físico: A temperatura ambiente (aproximadamente 25°C), el cloruro de sodio se presenta como un sólido cristalino blanco. Estos cristales tienen una estructura cúbica.
Punto de Fusión: El cloruro de sodio se funde a una temperatura relativamente alta, aproximadamente 801°C. Esto significa que se necesita una gran cantidad de energía para romper los fuertes enlaces iónicos que mantienen unidos los iones de sodio y cloruro en la red cristalina.
Punto de Ebullición: El cloruro de sodio hierve a una temperatura aún más alta, aproximadamente 1413°C. Se necesita aún más energía para separar las moléculas en fase gaseosa.
Densidad: La densidad del cloruro de sodio es de aproximadamente 2.16 g/cm³. Esto indica que es más denso que el agua.
Solubilidad: El cloruro de sodio es muy soluble en agua. Esto significa que se disuelve fácilmente en agua, formando una solución salina. La solubilidad aumenta ligeramente con la temperatura.
Conductividad Eléctrica: En estado sólido, el cloruro de sodio no conduce la electricidad porque los iones están fijos en la red cristalina. Sin embargo, cuando se disuelve en agua (formando iones libres) o se funde, se convierte en un buen conductor eléctrico.
Sabor: El cloruro de sodio tiene un sabor salado característico, que es fundamental para su uso como condimento en alimentos.
Propiedades Químicas del Cloruro de Sodio
Las propiedades químicas describen la capacidad de una sustancia para reaccionar con otras sustancias y transformarse en nuevas sustancias. Estas propiedades están relacionadas con la estructura atómica y los enlaces químicos del compuesto.
Estabilidad: El cloruro de sodio es un compuesto muy estable. No se descompone fácilmente a temperaturas normales. Tampoco reacciona fácilmente con el aire seco.
Reacción con Ácidos: El cloruro de sodio reacciona con ácidos fuertes, como el ácido sulfúrico (H₂SO₄), para producir cloruro de hidrógeno gaseoso (HCl), también conocido como ácido clorhídrico en solución acuosa, y sulfato de sodio (Na₂SO₄). Esta reacción es una fuente importante de ácido clorhídrico industrial.
Reacción con Nitrato de Plata: Cuando se agrega una solución de nitrato de plata (AgNO₃) a una solución de cloruro de sodio, se forma un precipitado blanco de cloruro de plata (AgCl). Esta reacción se utiliza para detectar la presencia de iones cloruro en una solución.
Electrólisis: La electrólisis de una solución acuosa de cloruro de sodio (salmuera) produce cloro gaseoso (Cl₂), hidrógeno gaseoso (H₂) e hidróxido de sodio (NaOH). Este proceso es fundamental en la producción industrial de cloro, sosa cáustica (hidróxido de sodio) e hidrógeno.
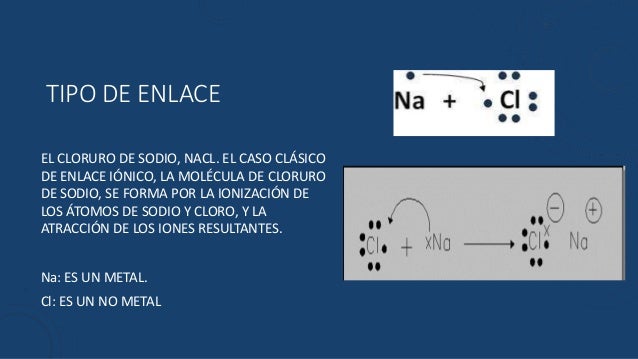
Enlace Iónico: El cloruro de sodio se forma a través de un enlace iónico. El átomo de sodio (Na) pierde un electrón para formar un ion sodio positivo (Na+), y el átomo de cloro (Cl) gana ese electrón para formar un ion cloruro negativo (Cl-). La atracción electrostática entre estos iones opuestos es lo que forma el enlace iónico y mantiene unidos los iones en la red cristalina.
En resumen, el cloruro de sodio posee propiedades físicas y químicas distintivas que lo hacen esencial tanto en la naturaleza como en diversas aplicaciones industriales. Su estabilidad, solubilidad y capacidad para conducir la electricidad en solución son solo algunas de las características importantes que definen este compuesto omnipresente.