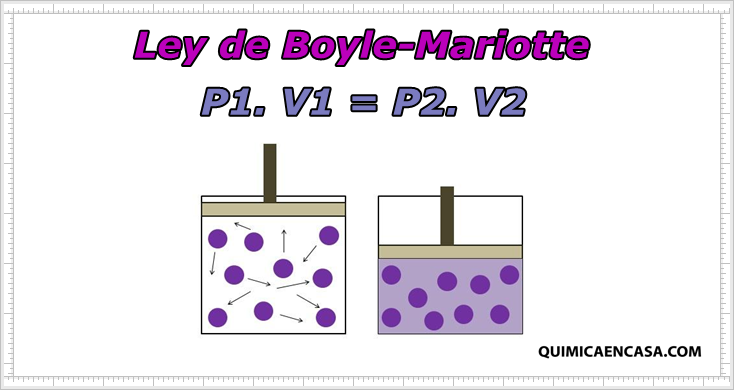
Características De La Ley De Boyle
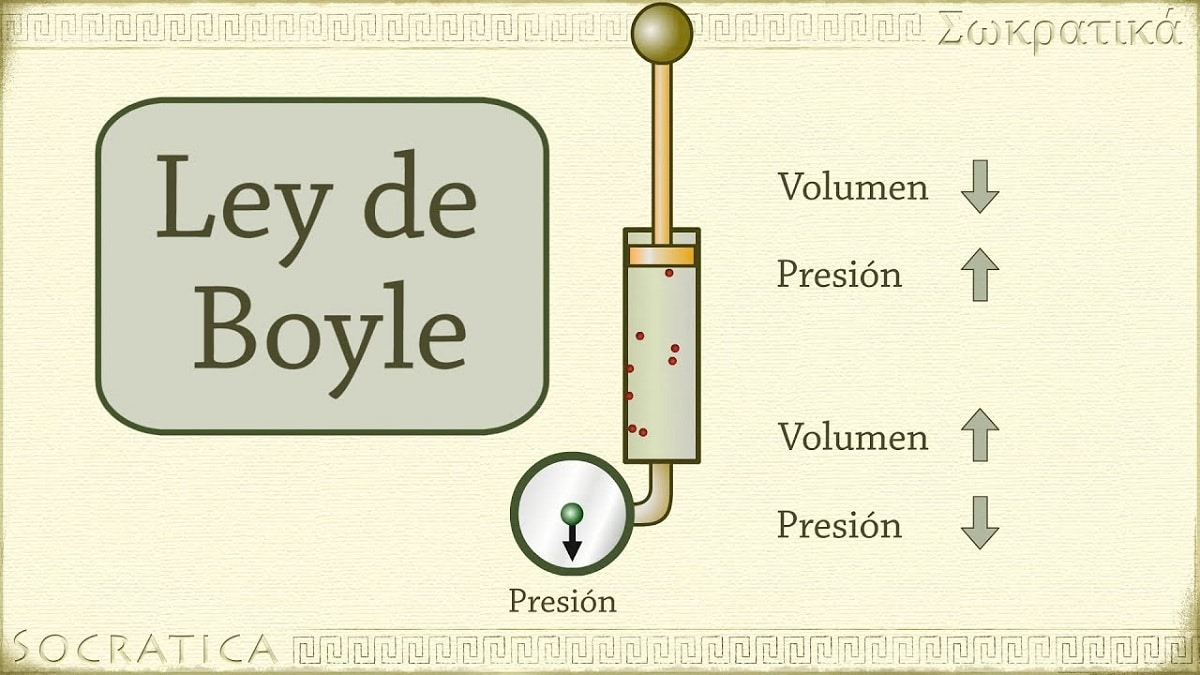
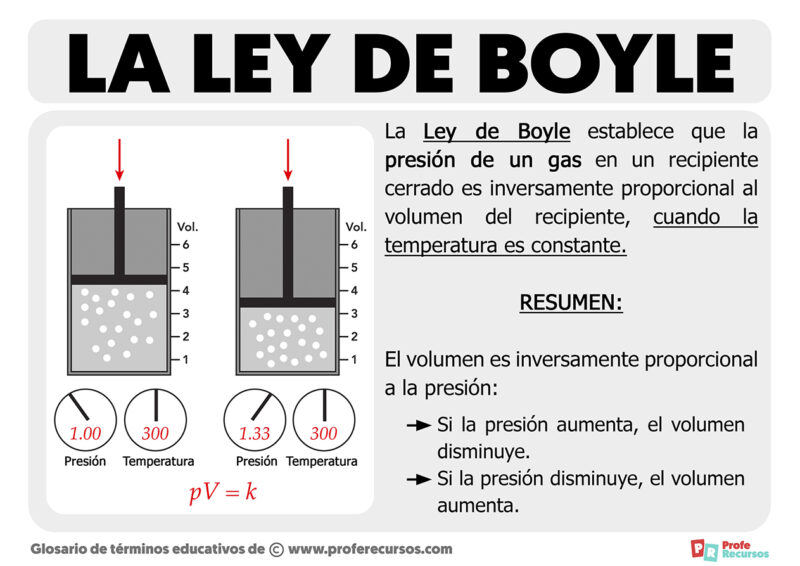
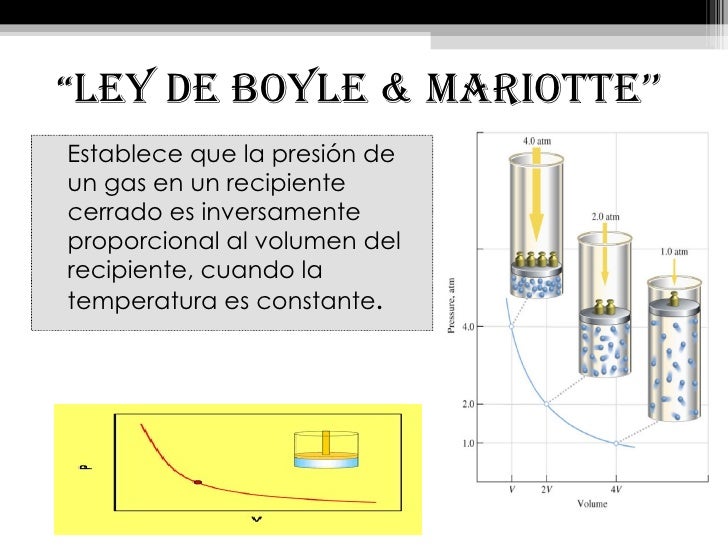
La Ley de Boyle describe la relación entre el volumen y la presión de un gas, siempre y cuando la temperatura y la cantidad de gas se mantengan constantes. En palabras sencillas: si reduces el volumen de un gas, su presión aumenta; y si aumentas el volumen, su presión disminuye.
¿Qué significa esto exactamente?
Analicemos la ley paso a paso:
- Volumen: Es el espacio que ocupa el gas. Imagina un globo. El volumen es cuánto aire cabe dentro del globo.
- Presión: Es la fuerza que ejerce el gas contra las paredes del recipiente que lo contiene. Piensa en el aire dentro de la llanta de un coche. La presión es lo que mantiene la llanta inflada y firme.
- Temperatura constante: La temperatura no debe cambiar durante el experimento. Debe ser la misma al principio y al final. Imagina inflar un globo; la temperatura del aire no debe subir ni bajar mucho durante el proceso.
- Cantidad de gas constante: No se añade ni se quita gas. Es como tener un globo sellado; no entra ni sale aire.
La fórmula de la Ley de Boyle
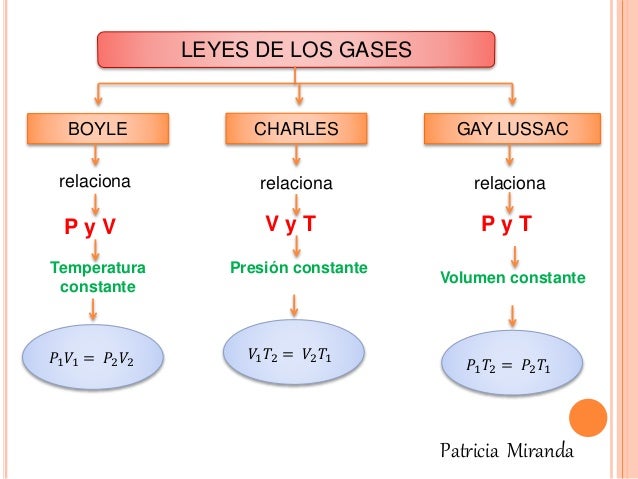
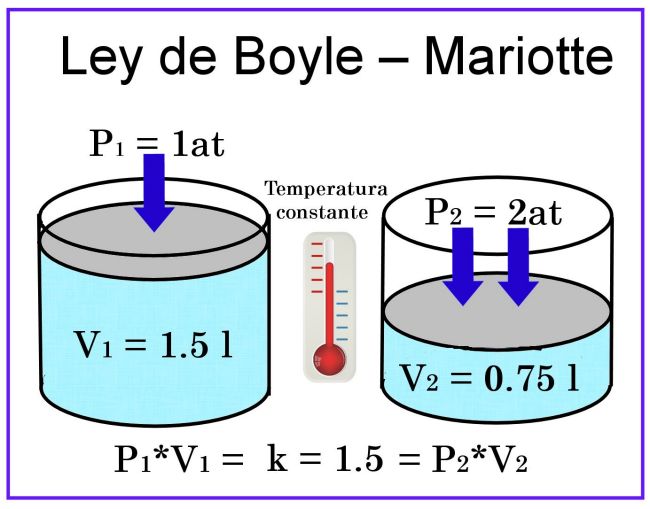
La Ley de Boyle se expresa con la siguiente fórmula: P₁V₁ = P₂V₂
Donde:
- P₁: Es la presión inicial.
- V₁: Es el volumen inicial.
- P₂: Es la presión final.
- V₂: Es el volumen final.
Esta fórmula indica que el producto de la presión y el volumen iniciales es igual al producto de la presión y el volumen finales. En otras palabras, la presión y el volumen son inversamente proporcionales.
Ejemplos de la Ley de Boyle en la vida real
La Ley de Boyle se observa en muchas situaciones cotidianas:
- Jeringa: Al empujar el émbolo de una jeringa (disminuyendo el volumen), la presión dentro de la jeringa aumenta.
- Inflar un neumático: Al bombear aire a un neumático, reduces el volumen disponible y aumentas la presión. Por eso se pone duro.
- Respiración: Cuando inspiramos, aumentamos el volumen de nuestros pulmones, lo que disminuye la presión del aire dentro de ellos. Esto permite que el aire entre. Cuando exhalamos, disminuimos el volumen, aumentando la presión, y el aire sale.
- Buceo: Los buceadores deben tener cuidado porque la presión aumenta con la profundidad. El volumen del aire en sus pulmones se reduce a medida que descienden, y deben exhalar para evitar daños.
En resumen
La Ley de Boyle es una regla fundamental de la física que explica cómo el volumen y la presión de un gas se relacionan cuando la temperatura y la cantidad de gas permanecen constantes. Es importante comprender esta ley para entender cómo funcionan muchos procesos a nuestro alrededor.