Aumento Del Punto De Ebullicion Pdf

El aumento del punto de ebullición es un fenómeno químico que describe cómo la temperatura a la que un líquido hierve se eleva cuando se le añade un soluto no volátil. En otras palabras, la presencia de un soluto hace que el líquido necesite más energía (y por lo tanto, una temperatura más alta) para transformarse en gas.
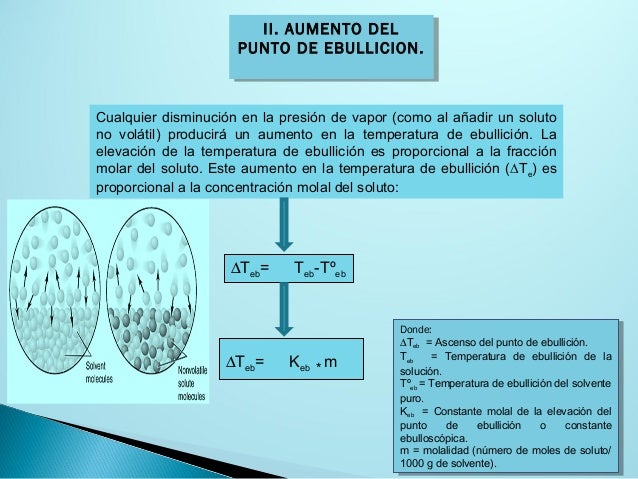
La idea principal detrás de esto es la disminución de la presión de vapor. Un líquido hierve cuando su presión de vapor iguala la presión atmosférica circundante. Al agregar un soluto, este interfiere con las moléculas del disolvente (el líquido), dificultando que escapen a la fase gaseosa. Esto reduce la presión de vapor del disolvente. Para que la presión de vapor vuelva a igualar la atmosférica y el líquido hierva, se necesita aumentar la temperatura.
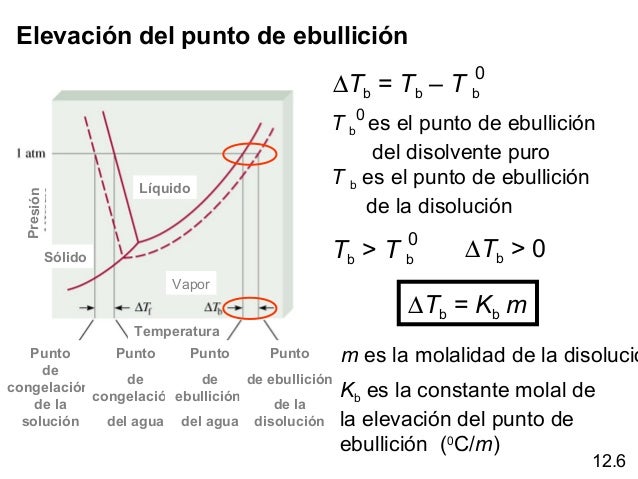
La cantidad de aumento en el punto de ebullición es directamente proporcional a la molalidad de la solución (moles de soluto por kilogramo de disolvente). La fórmula general es: ΔTb = Kb * m, donde ΔTb es el aumento en el punto de ebullición, Kb es la constante ebulloscópica del disolvente (un valor específico para cada disolvente, como el agua), y m es la molalidad.
Por ejemplo, si añadimos sal (NaCl) al agua, el punto de ebullición del agua aumentará. Cuanta más sal añadamos, mayor será el aumento. Esto explica por qué se añade sal al agua al cocinar pasta: aunque el aumento del punto de ebullición es pequeño, ayuda a cocinar la pasta ligeramente más rápido (y también la sazona).
Las aplicaciones prácticas son variadas. En la industria alimentaria, se utiliza para controlar las propiedades de cocción de soluciones. En la fabricación de anticongelantes, se añade un soluto (como etilenglicol) al agua para aumentar su punto de ebullición y disminuir su punto de congelación, protegiendo los motores de automóviles. Comprender el aumento del punto de ebullición nos permite controlar y predecir el comportamiento de las soluciones en diversas situaciones cotidianas e industriales.

+%3D+(+%2C83)°C.jpg)