Aportaciones De Erwin Schrödinger Al Modelo Atomico

Analicemos las contribuciones de Erwin Schrödinger al modelo atómico paso a paso. Consideremos qué supuestos hizo Schrödinger. Evalúemos las implicaciones de su trabajo. Intentaremos llegar a conclusiones lógicas.
Paso 1: Comprensión del Contexto
Inicialmente, debemos comprender el modelo atómico anterior al de Schrödinger. El modelo de Bohr fue un avance. Pero tenía limitaciones. No explicaba todos los fenómenos observados.
El modelo de Bohr asumía órbitas fijas para los electrones. Estas órbitas estaban cuantizadas. Esto significa que solo ciertos niveles de energía eran permitidos. Sin embargo, el modelo fallaba al aplicarse a átomos más complejos que el hidrógeno.
Paso 2: El Postulado de la Dualidad Onda-Partícula
Un concepto crucial es la dualidad onda-partícula. Louis de Broglie propuso que las partículas, como los electrones, tienen propiedades ondulatorias. Esto fue un cambio radical. Significaba que los electrones no solo eran partículas.
De Broglie sugirió que la longitud de onda de un electrón está inversamente relacionada con su momento. La ecuación es λ = h/p, donde λ es la longitud de onda, h es la constante de Planck y p es el momento. Schrödinger tomó esta idea como punto de partida.
Paso 3: La Ecuación de Schrödinger
La principal contribución de Schrödinger es su ecuación. Esta ecuación describe el comportamiento de las partículas subatómicas en términos de ondas. Es una ecuación diferencial que relaciona la energía total de una partícula con su energía cinética y potencial. La ecuación de Schrödinger, en su forma dependiente del tiempo, es: iħ∂ψ/∂t = Hψ.
Aquí, i es la unidad imaginaria, ħ es la constante de Planck reducida, ψ es la función de onda, t es el tiempo y H es el hamiltoniano, un operador que representa la energía total del sistema. La función de onda ψ contiene información sobre la probabilidad de encontrar un electrón en una región específica del espacio.
Paso 4: Interpretación de la Función de Onda
La interpretación física de la función de onda ψ es crucial. Max Born propuso que el cuadrado de la función de onda, |ψ|², representa la densidad de probabilidad. Esto significa que |ψ|²dV es la probabilidad de encontrar el electrón en un volumen dV alrededor de un punto.
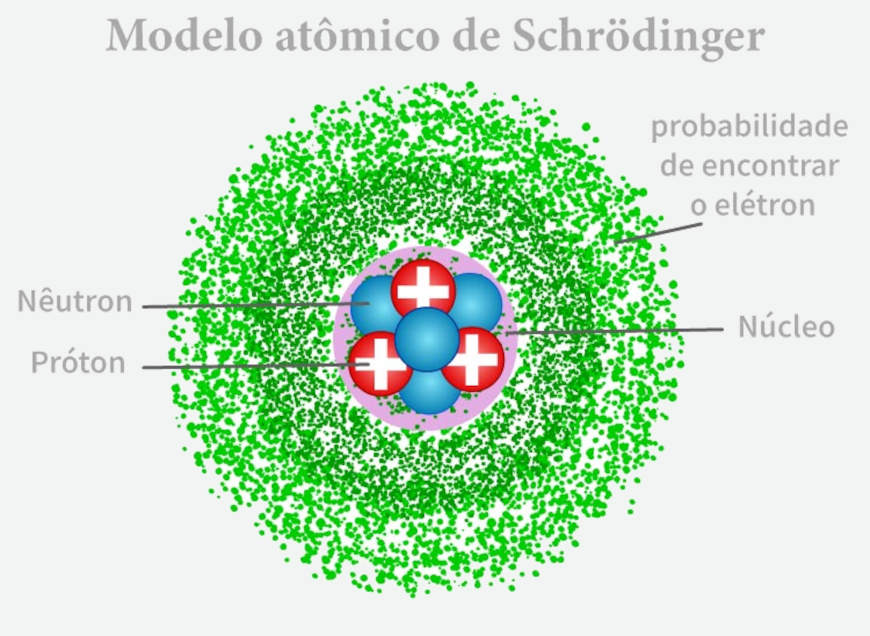
A diferencia del modelo de Bohr, donde los electrones seguían órbitas definidas, el modelo de Schrödinger describe regiones de probabilidad. Estas regiones se llaman orbitales. Los orbitales no son trayectorias fijas.
Paso 5: Resolución de la Ecuación de Schrödinger
Resolver la ecuación de Schrödinger para un átomo requiere matemáticas complejas. Para el átomo de hidrógeno, la ecuación se puede resolver analíticamente. Para átomos más complejos, se necesitan aproximaciones.
La solución de la ecuación proporciona un conjunto de números cuánticos. Estos números cuantifican la energía, el momento angular y la orientación espacial del electrón. Los números cuánticos son n, l, y ml.
Paso 6: Consecuencias del Modelo de Schrödinger
El modelo de Schrödinger tiene varias consecuencias importantes. Primero, explica el espectro de emisión del hidrógeno con gran precisión. Segundo, proporciona una base teórica para la tabla periódica.
El modelo también explica el enlace químico. Los orbitales atómicos se combinan para formar orbitales moleculares. Estos orbitales describen la distribución de los electrones en una molécula.
Paso 7: Limitaciones y Desarrollos Posteriores
A pesar de sus éxitos, el modelo de Schrödinger tiene limitaciones. No tiene en cuenta los efectos relativistas. Tampoco explica el espín del electrón directamente.
La ecuación de Dirac, que incorpora la relatividad especial, describe el comportamiento de los electrones de forma más precisa. La teoría cuántica de campos ofrece una descripción aún más completa.
Conclusión
Las aportaciones de Erwin Schrödinger al modelo atómico fueron revolucionarias. Su ecuación introdujo la mecánica cuántica en la descripción del átomo. Aunque el modelo ha sido refinado, su base permanece fundamental. Comprender su trabajo es esencial para la química y la física modernas.




/cloudfront-us-east-1.images.arcpublishing.com/abccolor/U3K5P673TBFCVOT73EQHPDDOAU.jpg)




